
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有______ 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的______. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有______,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | ______ | 固体中一定含有CaCO3 |

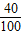 ×100%=1.2g,2.3g>1.2g,因此一定有氢氧化钙,即久置固体的成分是:Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
×100%=1.2g,2.3g>1.2g,因此一定有氢氧化钙,即久置固体的成分是:Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.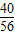 x+(2.3g-1.0g-x)×
x+(2.3g-1.0g-x)×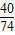 =2.0g×
=2.0g×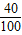 解得:x=0.56g
解得:x=0.56g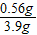 ×100%=14.4%.
×100%=14.4%.| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有 CaO 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的 稀盐酸. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有 Fe,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清的石灰水变浑浊 | 固体中一定含有CaCO3 |
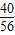 x+(2.3g-1.0g-x)×
x+(2.3g-1.0g-x)×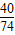 =2.0g×
=2.0g×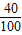 解得:x=0.56g
解得:x=0.56g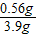 ×100%=14.4%.
×100%=14.4%.

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:初中化学 来源: 题型:阅读理解
| 品名:504双吸剂 成分:铁粉、生石灰等 |

| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有 氧化钙 氧化钙 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的 稀盐酸 稀盐酸 . |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有 铁 铁 ,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清的石灰水变浑浊 澄清的石灰水变浑浊 |
固体中一定含有CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 品名:504双吸剂 成分:铁粉、生石灰等 |
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不容物,溶液变红. | 固体中一定含有 CaO CaO 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的 稀盐酸 稀盐酸 . |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有 Fe Fe ,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清的石灰水变浑浊 澄清的石灰水变浑浊 |
固体中一定含有CaCO3 |

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管中,滴加足量的 稀盐酸 稀盐酸 . |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有 Fe Fe ,一定不含Fe2O3. |
| 实验操作 | 实验现象 | 实验结论 |
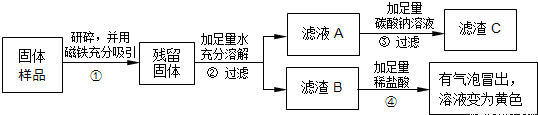
①取滤渣B于试管中,加入适量稀盐酸. ②将生成的气体通入澄清石灰水. ①取滤渣B于试管中,加入适量稀盐酸. ②将生成的气体通入澄清石灰水. |
①固体减少,有气泡冒出,溶液变为黄色. ②澄清石灰水变浑浊. ①固体减少,有气泡冒出,溶液变为黄色. ②澄清石灰水变浑浊. |
固体中一定含有CaCO3和Fe2O3. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 品名:504双吸剂 成分:铁粉、生石灰等 |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管中,滴加足量的 稀盐酸 稀盐酸 . |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有 Fe Fe ,一定不含Fe2O3. |

| 实验操作 | 实验现象 | 实验结论 |
①取滤渣B于试管中,加入适量稀盐酸. ②将生成的气体通入澄清石灰水 ①取滤渣B于试管中,加入适量稀盐酸. ②将生成的气体通入澄清石灰水 |
①固体减少,有气泡冒出,溶液变为黄色. ②澄清石灰水变浑浊. ①固体减少,有气泡冒出,溶液变为黄色. ②澄清石灰水变浑浊. |
固体中一定含有CaCO3 和Fe2O3. |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.
红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的 稀盐酸 稀盐酸 . |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有 Fe Fe ,一定不含Fe2O3. |

| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失 有气泡冒出,溶液变为黄色 有气泡冒出,溶液变为黄色 、澄清石灰水变浑浊 澄清石灰水变浑浊 |
固体中一定含有CaCO3 和Fe2O3. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com