【答案】
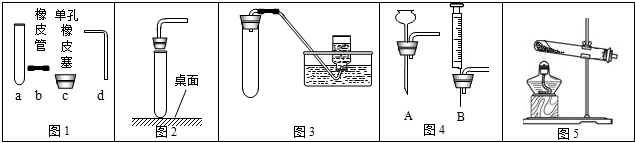
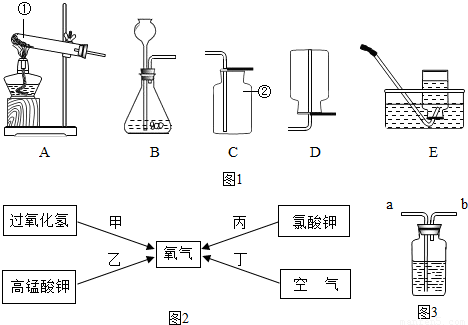
分析:(1)依据常用仪器回答;
(2)根据制取氧气的方法书写方程式;
(3)依据题意从实现原料和反应过程中的反应装置、反应条件的绿色化考虑甲、乙、丙三途径谁更能体现化学实验的绿色化追求.
(4)由高锰酸钾制取氧气时选择固态物质反应加热装置,注意用排水法收集完氧气后的先后操作顺序,避免操作失误造成不良后果;
(5)根据氯化铵固体与碱石灰固体共热来制取氨气需要加热以及氨气的性质为密度比空气小.NH
3极易溶于水来选择收集方法进行解答,并总结选择气体的收集方法需要考虑的因素;
(6)氧气不溶于水,氧气通入水中看气泡的多少,可以判断反应速率,且湿润氧气.
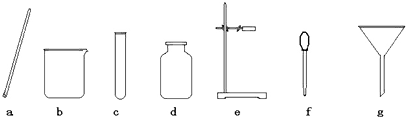
解答:解:(1)指定仪器分别是试管和氧气瓶;
(2)甲是利用双氧水和二氧化锰混合制氧气,方程式是:2H
2O
2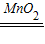
2H
2O+O
2↑;乙是利用高锰酸钾受热分解生成锰酸钾、二氧化锰、氧气,方程式是:2KMnO
4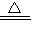
K
2MnO
4+MnO
2+O
2↑;
(3)制取装置包括加热和不需加热两种,用双氧水制氧气不需要加热,可以节约热能,且另一种生成物是水,无污染,所以符合绿色化学的理念;用高锰酸钾或氯酸钾制氧气需要加热,消耗能源,不符合绿色化学的理念.故选甲;
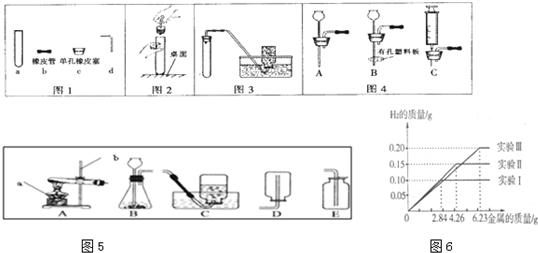
(4)加热高锰酸钾制取氧气属于固体加热型,故选发生装置A;用排水法收集氧气完毕后,停止加热时要移导管后熄灯,防止试管温度降低,压强减小,水槽中的水倒吸入试管引起试管炸裂;
(5)用氯化铵固体与碱石灰固体共热来制取氨气属于固体加热型,故选发生装置A;氨气密度比空气小,极易溶于水,故只能用向下排空气法收集;选择气体收集方法时,通常需要考虑气体的密度和溶解性;
(6)氧气从a进入水后,由于氧气不易溶于水,会从b管导出.这样能看到是否有氧气输出和氧气的输出速率,并能湿润氧气;
故答案为:(1)试管;集气瓶;
(2)2H
2O
2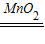
2H
2O+O
2↑;2KMnO
4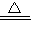
K
2MnO
4+MnO
2+O
2↑;
(3)甲;
(4)A;将导管从水槽中移出;熄灭酒精灯;
(5)A;D;气体的密度;气体的溶解性;
(6)观察是否有氧气输出(或者观察输出氧气的速率或增加氧气的湿度…).
点评:此题主要考查根据反应物状态和反应条件选择实验室制取氧气、氨气的实验装置,根据收集气体的性质选择收集方法及注意事项,此题设计开放,能较好锻炼学生的思维能力.

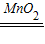 2H2O+O2↑;乙是利用高锰酸钾受热分解生成锰酸钾、二氧化锰、氧气,方程式是:2KMnO4
2H2O+O2↑;乙是利用高锰酸钾受热分解生成锰酸钾、二氧化锰、氧气,方程式是:2KMnO4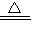 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;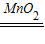 2H2O+O2↑;2KMnO4
2H2O+O2↑;2KMnO4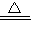 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;

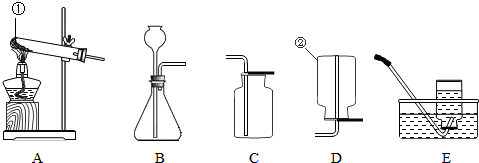
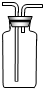
 20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答:
20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答: