一瓶久置的固体氢氧化钠,部分变质为Na2CO3.为测定该瓶固体中氢氧化钠的质量分数,取样20g配成溶液,加人足量的CaCl2溶液,得到白色沉淀10g.
(1)氢氧化钠变质的原因是______.
(2)计算该瓶固体中氢氧化钠的质量分数.
【答案】
分析:(1)由氢氧化钠能够与二氧化碳的性质分析解答;
(2)根据沉淀的质量利用方程式可以求出碳酸钠的质量,进而可求出固体中氢氧化钠的质量,从而可知该瓶固体中氢氧化钠的质量分数;
解答:解:由于氢氧化钠在空气中能与空气中的二氧化碳反应生成碳酸钠,所以易变质;
(2)设样品中碳酸钠的质量是x
Na
2CO
3+CaCl
2=CaCO
3↓+2NaCl
106 100
x 10g
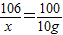
x=10.6g
所以原固体中氢氧化钠的质量是20g-10.6g=9.4g
所以固体中氢氧化钠的质量分数为

故答案为:(1)氢氧化钠与空气中的二氧化碳反应生成了碳酸钠;
(2)该瓶固体中氢氧化钠的质量分数为47%;
点评:本题主要考查学生运用化学方程式和质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

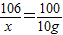




 则该溶液中双氧水的溶质质量分数是多少?
则该溶液中双氧水的溶质质量分数是多少?