
 如图是某元素在元素周期表中的信息,据图回答:
如图是某元素在元素周期表中的信息,据图回答: 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:

| A、除去A中混有的少量B,可采用降温结晶的方法 |
| B、50℃时A的饱和溶液中,溶质的质量分数为50% |
| C、将C的饱和溶液变为不饱和溶液,可采用升高温度的方法 |
| D、将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、分子是化学变化中的最小粒子 |
| B、氧气和臭氧(O3)都是由同种元素组成的 |
| C、H元素和O元素质子数不同 |
| D、在化学变化中分子可以再分 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、空气中含量最多的物质是氧气 |
| B、密度最小的气体是氦气 |
| C、天然存在的最硬的物质是金刚石 |
| D、地壳中含量最多的元素是铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
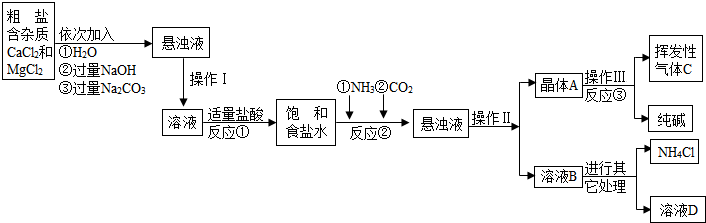
| ||
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
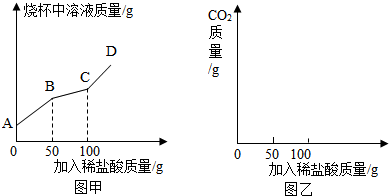
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com