医学上经常用硫酸亚铁糖衣片给贫血患者补铁.某兴趣小组的同学对糖衣片中硫酸亚铁晶体(FeSO
4?xH
2O)的组成进行了探究.
【查阅资料】
(1)白色的无水硫酸铜粉末遇水会变成蓝色的硫酸铜晶体.
(2)硫酸亚铁晶体加热先失去结晶水,高温继续分解产生一种金属氧化物和两种非金属氧化物.
(3)能使高锰酸钾溶液褪色的气体有二氧化硫、乙烯(C
2H
4)等.
(4)亚铁离子遇具有氧化性的物质易被氧化成铁离子.
【进行实验】
该兴趣小组同学称取ag硫酸亚铁晶体(FeSO
4?xH
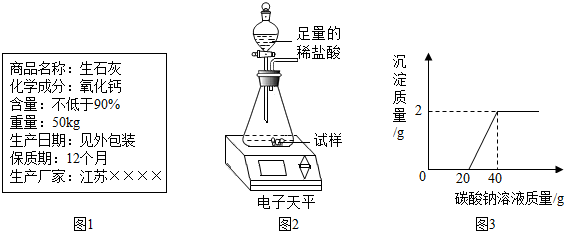
2O)样品按图1装置高温加热,使其完全分解,并对所得产物进行分析,利用SDTQ600热分析仪对硫酸亚铁晶体热分解获得相关数据,绘制成图2所示关系图.

【数据分析】
(1)图1装置B中无水硫酸铜粉末变蓝,质量增加12.6g,说明产物中有(填化学式,下同)
;装置C中高锰酸钾溶液褪色,说明产物中还有
;
(2)T
4℃时,硫酸亚铁晶体经完全分解后装置A中固体呈红色,放入足量稀盐酸,固体全部溶解,得到黄色溶液,则装置A中红色固体是
;
(3)兴趣小组的同学从理论上分析硫酸亚铁分解还生成另一物质SO
3,写出FeSO
4分解的化学方程式
;
(4)请根据上述实验及图2中有关数据计算FeSO
4?xH
2O中的x.(写出计算过程)
【交流讨论】
(1)反应完全后仍要持续通入氮气,否则测出的x值会(填“偏大”“偏小”或“不变”)
;
(2)硫酸亚铁糖衣片的糖衣除了用于包装药物外,还可能具有的作用是
.




 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案
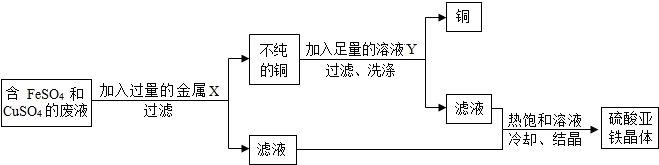
 某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如图实验:
某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如图实验: