
(7分)“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气。实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分及其质量。
【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【查阅资料】
①2Na2O2+2H2O═4NaOH+O2↑ 2Na2O2+2CO2═2Na2CO3+O2
②碳酸钠溶液显碱性,氯化钙溶液显中性。
③Na2CO3+ CaCl2═CaCO3↓+2 NaCl
【猜想与假设】
(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是________________________的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
……
【设计实施方案】
| 实验步骤 | 实验现象 |
| ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体。 | 固体完全溶解,______________________ |
| ②继续向上述试管中加入足量的石灰水,充分反应。 | __________________________________ |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g。 | |
| | Na2O2 | NaOH | Na2CO3 |
| 成分(填“有”或“没有”) | | | |
| 质量(g) | | | |
【猜想与假设】
(2)Na2O2和Na2CO3
【设计实施方案】
【解释与结论】实验操作 实验现象 固体完全溶解,有气泡产生,带火星木条复燃。 产生白色沉淀
【反思与评价】 Na2O2 NaOH Na2CO3 成分(填“有”或“没有”) 有 有 有 质量(g) 1.56 0.38 1.06
(1)密封保存(隔绝水或二氧化碳)
(2)不合理,因为过氧化钠与水反应也能生成氢氧化钠,也能使无色酚酞试液变红,所以,不能证明原粉末中有NaOH。
解析试题分析:【猜想与假设】(2)粉末成分是Na2O2和Na2CO3的混合物。
【设计实施方案】
【解释与结论】实验步骤 实验现象 ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体。
固体完全溶解,有气泡产生,带火星木条复燃。②继续向上述试管中加入足量的石灰水,充分反应。 产生白色沉淀 ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g。
粉末中含有的成分及质量
【反思与评价】 Na2O2 NaOH Na2CO3 成分(填“有”或“没有”) 有 有 有 质量(g) 1.56 0.38 1.06
(1)实验室在保存过氧化钠时应注意密封保存。
(2)若把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH,则该方案不合理,因为过氧化钠与水反应也能生成氢氧化钠,也能使无色酚酞试液变红,所以,不能证明原粉末中有NaOH。
考点:物质推断;过氧化钠的性质;酸碱指示剂;实验设计与探究。
点评:推断物质,要根据物质的性质,设计合理的实验方案,根据反应的不同现象来区分;无色酚酞试液,遇到酸性的物质不变色,遇到碱性的物质变红色。


 备战中考寒假系列答案
备战中考寒假系列答案科目:初中化学 来源: 题型:

| A | B | C | D | |
| X | 化合反应 | 置换反应 | 化合物 | 钠盐 |
| Y | 氧化反应 | 复分解反应 | 氧化物 | 碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样品少量于试管中,加入适量水,震荡,样品全部溶于水,向其中加入无色酚酞溶液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取样品少量于试管中,加入适量水,震荡,样品全部溶液水,向其中加入足量的 CaCl2溶液 CaCl2溶液 |
出现白色沉淀 | 白色物质是 Na2CO3 Na2CO3 |
| ②静止片刻,向上层清液中滴加无色酚酞溶液 | 无明显现象 |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
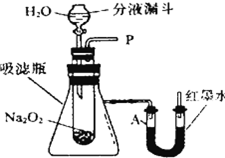 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.查看答案和解析>>
科目:初中化学 来源:2012年湖南省株洲市攸县中考化学模拟试卷(二)(解析版) 题型:解答题
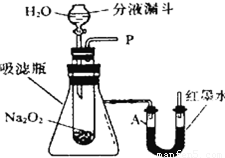
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com