【答案】
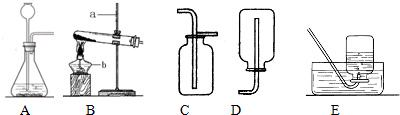
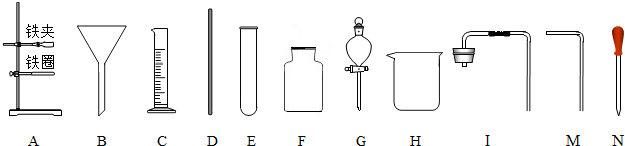
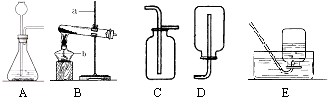
分析:(1)根据对常见的仪器的认识和作用进行解答;
(2)根据反应物的状态和反应条件选择发生装置,根据反应原理书写表达式,二氧化锰在反应中起催化作用;
(3)根据反应物的状态和反应条件选择发生装置,根据反应原理书写表达式;
(4)根据实验现象分析二氧化碳的性质及其用途;
(5)根据实验目的及二氧化碳的水溶性进行分析植物油的作用,根据排水法测气体的体积的原理判断空气的影响;
(6)根据实验室制取二氧化碳的装置的注意事项进行分析,并对C同学改进的装置进行评价.
解答:解:(1)根据对仪器的性状和作用可以判断a是铁架台,起转移仪器的作用,b是酒精灯,主要用来给物质加热;
故答案为:铁架台;酒精灯;
(2)实验室用过氧化氢和二氧化锰混合制取氧气时,该反应不需加热,所以应选用的发生装置是A;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的文字表达式是:过氧化氢
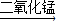
水+氧气;
故答案为:A;过氧化氢
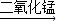
水+氧气;催化;
(3)实验室制取二氧化碳是用大理石和稀盐酸反应,由于反应是固体和液体常温下制备气体,所以发生装置选择A;二氧化碳气体的密度大于空气,因为其溶于水,不能采用排水法收集,故只能用向上排空气收集;大理石的主要成分碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应的文字表达式是:碳酸钙+盐酸→氯化钙+水+二氧化碳;
故答案为:A; C; 碳酸钙+盐酸→氯化钙+水+二氧化碳;
(4)向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳气体的密度大于空气,且二氧化碳不能燃烧、也不能支持燃烧;因此,二氧化碳可用于灭火;
故答案为:密度大于空气;不能燃烧、也不支持燃烧;灭火;
(5)二氧化碳能溶于水,所以要在水的上方放一层植物油,防止二氧化碳溶于水;排水法测气体体积的原理是利用排出水的体积和进入装置中的气体的体积相等的原理进行的,所以在没有二氧化碳生成时,盛水的集气瓶中压强和外界大气压是相等,当有二氧化碳气体生成时,集气瓶内气体压强增大,将水排出,所以油上方的空气对实验结果没有影响;
故答案为:防止二氧化碳溶于水且与水反应;无;
(6)甲装置中漏斗的底端应该伸到液面以下,否则生成的二氧化碳会从漏斗的底端跑到空气中,从而浪费较多的盐酸;C同学在漏斗下端套上一个破试管,相当于把漏斗的底端伸入到液面里,所以能收集到反应制取的所有二氧化碳,节约了药品,也进行了废物再利用(破试管),能解决AB同学所提出的问题;
故答案为:二氧化碳会从漏斗逸出;能;节约药品(合理均可).
点评:本题主要考查学生对实验室制备氧气和二氧化碳的反应原理、发生装置的选择、收集装置的选择及有关气体体积测定方法况,能很好的考查学生掌握和应用.

 水+氧气;
水+氧气; 水+氧气;催化;
水+氧气;催化;