
氯化钠是一种重要的资源,在海水中储量很丰富。
(1)海水晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程(如图1)。已知B溶液恰好是氯化钠的饱和溶液,与B溶液中溶质质量相等的溶液是________(填字母,下同),与B溶液中溶质质量分数相等的溶液是________。
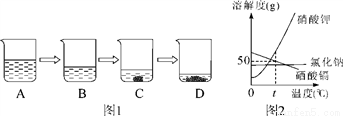
(2)氯化钠、硝酸钾、硒酸镉的溶解度曲线如图2所示。据图回答:
①溶解度变化受温度影响最大的是________,t℃时,溶解度最小的是________;
②t℃时,将25g硒酸镉加入________g水中,完全溶解后,恰好得到饱和溶液。要进一步提高该溶液的溶质质量分数,可进行的操作是_________________________;
③硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是____________________。
科目:初中化学 来源:广东省佛山市南海区2018届九年级上学期期末考试化学试卷 题型:综合题
为了除去二氧化碳中的少量氧气,并探究二氧化碳的性质,某同学设计了如图所示这套装置。
实验步骤 | 实验现象 | 现象分析 |
①点燃A处酒精灯,缓缓通入混合气体 | A中硬质玻璃管内固体 ___,B、C、D无明显现象,E中石灰水变浑浊。 | A硬质玻璃管中铜粉的作用是_____。E中发生反应的化学方程式是___。 |
②点燃B中酒精喷灯 | B中木炭粉减少,E中石灰水浑浊,液面下降。 | B硬质玻璃管中发生反应的化学方程式是_____。 |
③点燃C中酒精灯 | C中现象___,E中石灰水变澄清,液面下降 | C硬质玻璃管中发生反应的化 学方程式是__ |
④停止通入混合气体,并用止水夹夹紧进气口,熄灭A,B,C处的酒精灯和酒精喷灯 | ___ 处有液体导入(填A﹣F) | D装置的作用是__ |
【拓展与思考】
(1)从步骤②开始E中液面开始下降的原因:_____
(2)有同学认为该装置需要添加尾气处理理装置,你认为是否需要并说明理由:_____。
查看答案和解析>>
科目:初中化学 来源:河南省南阳市内乡县2018届九年级上学期期末质量评估化学试卷 题型:单选题
实验室制取某些气体的装置如图。下列说法正确的是
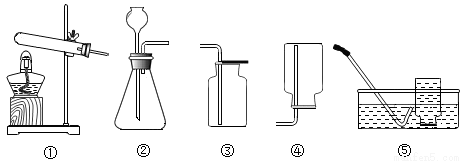
A. 装置①和⑤组合可以用来制取氧气 B. 装置②和③组合可以用来制取氢气
C. 装置②和④组合可以用来制取二氧化碳 D. 装置②可以较好地控制反应速率
查看答案和解析>>
科目:初中化学 来源:人教版2018届九年级下册化学单元测试:第8单元 金属和金属材料 题型:单选题
将一定质量的铁粉加至H2SO4、MgSO4和CuSO4的混和溶液中,充分反应后过滤,得到滤液M和滤渣N,下列有关说法中,不合理的是
A. 滤液M中一定存在Fe2+
B. 滤渣N的质量一定小于加入铁粉的质量
C. 滤渣N中一定没有单质镁
D. 滤液M中至少含有两种金属阳离子
查看答案和解析>>
科目:初中化学 来源:人教版2018届九年级下册化学单元测试:第9单元 溶液 题型:单选题
小明在实验操作技能考试中抽中的题目是“用固体氯化钠配制50g溶质质量分数为6%的氯化钠溶液”。他的有关做法正确的是( )
A. 选择的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、试剂瓶
B. 将氯化钠直接放在托盘天平左盘上称量3.0g
C. 用100mL量筒量取所需水的体积
D. 用内壁附有水珠的烧杯配制溶液
查看答案和解析>>
科目:初中化学 来源:人教版2018届九年级下册化学单元测试:第9单元 溶液 题型:单选题
某温度下,在100g质量分数为20%的KNO3不饱和溶液甲中加入10gKNO3固体,恰好得到饱和溶液乙。下列说法正确的是( )
A. 该温度下,KNO3的溶解度为30g
B. 乙溶液的质量分数为30%
C. 降低温度,可以使甲溶液变成饱和溶液
D. 升高温度,甲、乙两溶液的质量分数都增大
查看答案和解析>>
科目:初中化学 来源:人教版2018届九年级下册化学单元测试:第10单元 酸和碱 题型:单选题
小凯整理归纳得出的规律合理的是( )
A. 溶液中的溶剂一定是水
B. 水既能跟某些金属氧化物反应生成碱,也能跟某些非金属氧化物反应生成酸
C. 酸、碱中一定都含有氧元素
D. 不能使酚酞溶液变红的溶液一定是酸溶液
查看答案和解析>>
科目:初中化学 来源:石家庄新世纪外国语学校2017-2018年度九年级第一学期第三次质量检测化学试卷 题型:简答题
下图表示有关物质的转化关系(反应条件及部分生成物已省略)。已知甲、乙、丙为单质,其它均为化合物,A、C都是无色液体,且所含元素种类完全相同:D是无色有毒气体。
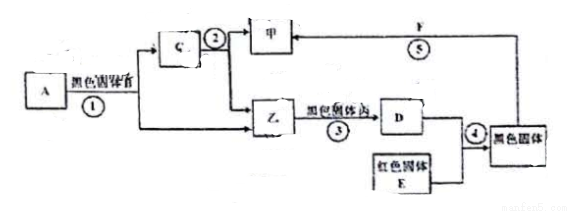
(1)F的化学式可能为(填一个即可)________。
(2)反应②的化学方程式________。
(3)反应④的化学方程式__________。
(4)反应①-⑤中属于分解反应的是_______________(填序号)。
(5)反应⑤的现象为___________。
【答案】 HCl或H2SO4 2H2O 2H2↑+O2↑
2H2↑+O2↑  ①②色 有气泡产生,溶液由无色变为浅绿、黑色固体减少
①②色 有气泡产生,溶液由无色变为浅绿、黑色固体减少
【解析】本题是推断题,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证。
A与C的组成元素相同的液体,乙为单质,可判断A为过氧化氢、 C为水,乙为氧气;由C分解生成氧气和甲,则甲是氢气;根据丙为黑色粉末且D是无色有毒气体,丙是碳,则D是一氧化碳;一氧化碳与红色固体E反应生成黑色固体,则红色固体为氧化铁,黑色固体是铁,铁能与酸溶液反应生成氢气 ,则F为酸溶液,可能为稀硫酸或稀盐酸,代入框图,假设合理。因此:
(1)F是硫酸或盐酸,化学式为HCl或H2SO4;
(2)反应②是水在通电条件下生成了氧气和氢气,化学方程式是2H2O 通电 2H2↑+ O2 ↑ ;
(3)反应④是一氧化碳和氧化铁在高温条件下生成了二氧化碳和铁,化学方程式是 ;
;
(4)反应①-⑤中①②都是由一种物质生成两种物质,属于分解反应;。
(5)反应⑤是铁与酸溶液反应的现象为有气泡产生,溶液由无色变为浅绿色,黑色固体减少
。
【题型】推断题
【结束】
35
小明过生日,吹蜡烛时怎么吹也吹不灭,小明同学带着疑问与化学兴趣小组的老师和同学一起对“吹不灭的蜡烛”展开了探究。
【查阅资料】普通蜡烛由石蜡和蜡烛芯制成,而吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末,打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃,当蜡烛吹灭后,未冷却的金属继续燃烧,从而使蜡烛复燃。吹不灭的蜡烛芯外的金属可能是镁、铝、铁或铜中的一种,为确定该金属的成分,他们进行了下面的探究。(不考虑打火石中稀土元素对探究金属性质的影响)
【提出问题】“吹不灭蜡烛”打火石中含有哪种金属?
【做出猜想】
猜想一:该金属是Cu 猜想二:该金属是Fe
猜想三:该金属是Mg 猜想四:该金属是Al
【实验探究】同学们根据所学的化学知识设计并进行如下实验确定该金属的成分.
(1)甲同学切开蜡烛,取出打火石,用砂纸打磨,打火石呈银白色,猜想一不成立,原因是_________。
(2)乙同学取少量打磨后的打火石于试管中,滴加稀盐酸,观察现象,经过对现象的分析后,他们认为该金属一定不是铁,他们观察到的现象是_______,猜想二不成立。
(3)为了进一步确定该金属的种类,小明提议用硫酸铜溶液进行试验,请你预测,将打火石加入到硫酸铜溶液后的现象是__________,其中涉及到的化学方程式______________。(任写一个即可)
(4)同学们一致认为小明的方案不合理,经过讨论他们设计了下面的实验方案,确认了打火石中的金属是镁。
操作步骤 | 实验现象 | 实验结论 |
取一块打磨后的“打火石”于试管中,加入少量__________溶液 | “打火石”表面有银白色固体析出 | “打火石”中的金属是Mg |
有关的化学方程式为_______________________。
【交流与反思】这种蜡烛燃烧时,蜡烛芯里的金属为什么不燃烧?_______________,
这种蜡烛实际也可以熄灭,可采用的方法是_____________(填一种即可)。
【答案】 铜为紫红色 溶液为无色 打火石表面有红色固体附着,溶液颜色变浅(或变为无色) Mg+CuSO4=MgSO4+Cu或2Al+3CuSO4=Al2(SO4)3+3Cu(任写一个即可) 硫酸铝 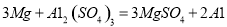 蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以然烧 隔绝氧气 或剪除灯芯 或用湿抹布盖灭、用沙土盖灭等(其他合理答案均可)
蜡烛烛芯被石蜡蒸汽包围着,缺少氧气,里面的金属难以然烧 隔绝氧气 或剪除灯芯 或用湿抹布盖灭、用沙土盖灭等(其他合理答案均可)
【解析】本题考查了金属的性质和物质燃烧的条件。
(1)甲同学切开蜡烛,取出打火石,用砂纸打磨,打火石呈银白色,猜想一不成立,原因是铜为紫红色;
(2)铁与稀盐酸反应会生成浅绿色溶液。乙同学取少量打磨后的打火石于试管中,滴加稀盐酸,观察现象,经过对现象的分析后,他们认为该金属一定不是铁,他们观察到的现象是溶液为无色,猜想二不成立;
(3)铝和镁的活动性都大于铜,都能将硫酸铜中铜置换出来,生成硫酸铝或硫酸镁,所以可预测,将打火石加入到硫酸铜溶液后的现象是打火石表面有红色固体附着,溶液颜色变浅(或变为无色),其中涉及到的化学方程式2Al+3CuSO4=Al2(SO4)3+3Cu或Mg+CuSO4=MgSO4+Cu;
(4)镁的活动性大于铝,镁能将铝盐溶液中的铝置换出来。取一块打磨后的“打火石”于试管中,加入少量硫酸铝溶液,该反应是镁与硫酸铝反应生成硫酸镁和铝,化学方程式是: 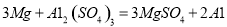 ;蜡烛芯里的金属不燃烧原因是蜡烛烛芯被石蜡蒸汽包围着,缺少氧气里面的金属难以然烧;熄灭蜡烛可采用的方法是隔绝氧气 或剪除灯芯 或用湿抹布盖灭、用沙土盖灭等(其他合理答案均可)。
;蜡烛芯里的金属不燃烧原因是蜡烛烛芯被石蜡蒸汽包围着,缺少氧气里面的金属难以然烧;熄灭蜡烛可采用的方法是隔绝氧气 或剪除灯芯 或用湿抹布盖灭、用沙土盖灭等(其他合理答案均可)。
【题型】科学探究题
【结束】
36
某化学兴趣小组同学为回收一块质量为40 g的铜锌合金中的铜,将该合金放人烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸100 g,烧杯内剩余固体27 g。请完成下列计算:
(1)40 g铜锌合金中锌的质量是________g 。
(2)计算所用稀硫酸中溶质的质量分数为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com