
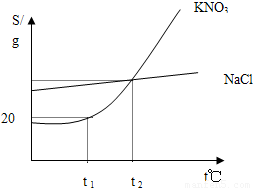
 ×100%,所以饱和溶液的质量分数取决于溶解度的大小,因为t2℃KNO3 的溶解度等于氯化钠的溶解度,所以饱和溶液的溶质质量分数相等,故C错;
×100%,所以饱和溶液的质量分数取决于溶解度的大小,因为t2℃KNO3 的溶解度等于氯化钠的溶解度,所以饱和溶液的溶质质量分数相等,故C错;

科目:初中化学 来源: 题型:
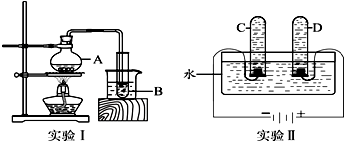
 (2010?南宁)如右图所示,当打开分液漏斗上的活塞让水滴入大试管中,可观察到以下现象:
(2010?南宁)如右图所示,当打开分液漏斗上的活塞让水滴入大试管中,可观察到以下现象:查看答案和解析>>
科目:初中化学 来源: 题型:
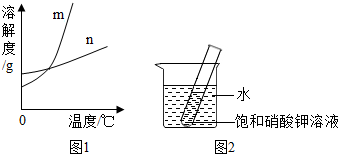
 某固态混合物中含有m g KNO3和若干克不溶于水的杂质,将此混合物加入n g水中,在10℃,40℃,75℃时观察,充分溶解后的结果如表所示.KNO3的溶解度曲线见图.
某固态混合物中含有m g KNO3和若干克不溶于水的杂质,将此混合物加入n g水中,在10℃,40℃,75℃时观察,充分溶解后的结果如表所示.KNO3的溶解度曲线见图.| 温度(℃) | 10 | 40 | 75 |
| 未溶固体质量(g) | 261 | 175 | 82 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
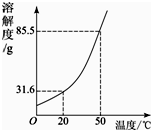
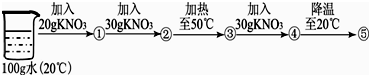
查看答案和解析>>
科目:初中化学 来源: 题型:解答题




查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com