
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:单选题
人类的日常生活和工农业生产离不开水,下列说法正确的是( )
A. 无法用水鉴别硝酸铵、氢氧化钠两种固体
B. 用水浇灭着火的纸箱,其原理是移除了可燃物
C. 天然水经过自然沉降、过滤、吸附,即得纯水
D. 使用加有洗涤剂的水可去除衣服上的油污
D 【解析】A、硝酸铵、氢氧化钠两种固体溶于水分别吸热、放热,温度分别降低、升高,可以鉴别,错误;B、用水浇灭着火的纸箱,其原理是使温度降到着火点以下,错误; C、天然水经过自然沉降、过滤、吸附,不能除去水中的可溶性钙镁化合物,不能得到纯水,错误;D、洗涤剂具有乳化作用,使用加有洗涤剂的水可去除衣服上的油污,正确。故选D。查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:单选题
下列4个图像中,能正确反应变化关系的是
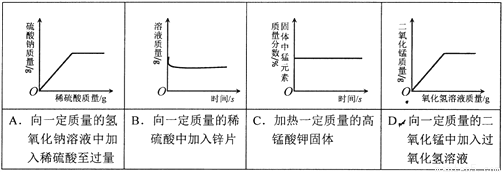
A. A B. B C. C D. D
A 【解析】A、稀硫酸与氢氧化钠溶液反应生成硫酸钠和水,当氢氧化钠反应完以后,硫酸钠的质量不再增大,正确;B、向一定质量的稀硫酸中加入锌片,溶液质量逐渐增多,当稀硫酸完全反应后,溶液质量不再增多,错误;C、化学反应前后固体中锰前后元素的质量不变,但反应后固体质量减少,所以随着反应的进行,固体中锰元素的质量逐渐增多,当反应结束后,固体中锰元素的质量不再改变,错误;D、在过氧化氢溶液分解反应中,...查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:多选题
“细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是
[Failed to download image : http://qbm-images.oss-cn-hangzhou.aliyuncs.com/QBM/2018/4/15/1924397705895936/1924665888735232/STEM/3b8a8fbdbd794f79ab3e1d573675dbcd.png]
A. 反应①化学方程式:4FeS2+15O2+2X=2Fe2(SO4)3+2H2SO4,X为H2O
B. 整个流程提高了能量的利用率
C. 图中有机物一定不含氧元素
D. 氧化铁硫杆菌在反应①中起催化作用
C 【解析】A、由4FeS2+15O2+2X=2Fe2(SO4)3+2H2SO4可知,反应前后铁原子都是4个,硫原子都是8个,反应后氧原子是32个,反应前应该是32个,其中2个包含在2X中,反应后氢原子是4个,反应前应该是4个,包含在2X中,因此X为H2O,该选项说法不正确;B、借助利用氧化铁硫杆菌促使FeS2氧化成硫酸铁和硫酸释放的能量供给二氧化碳和水的反应,提高了能量的利用率,该选项说法...查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:填空题
化学就在身边,我们的衣、食、住、行都离不开它。请回答下列问题:
(1)妈妈买了一件羊毛上衣,小红怀疑衣服面料成分是合成纤维,她采用的鉴别方法是______。
(2)妈妈为小红准备了米饭、红烧肉、高钙牛奶,请从营养均衡的角度考虑,妈妈还应增加____________或水果以补充营养素_______(填字母)。
A.糖类 B.蛋白质 C.油脂 D.维生素
(3)细心的小红发现铝制门窗比较耐腐蚀,主要原因是______(用文字叙述)。小红还发现新买的家具带有异味,于是在室内放了几个活性炭包以达到除去异味的目的,这是利用了活性炭的______性。
(4)近几年,由于汽车数量急剧增加、工业快速发展等因素,致使化石燃料大量使用,对环境的影响也日益凸显。小红查阅资料后获知:科学家在积极寻找洁净的新能源过程中,发现了氨气燃烧能释放出大量的热且产物对环境没有污染,其反应的微观示意图如下,该反应的化学方程式为________________________。
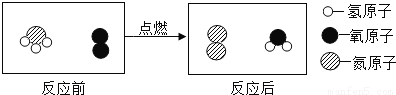
查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:填空题
写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。
(2)工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应:_______________________。工业炼铁的主要设备是___________________________。
(3)车用乙醇汽油不但可以节省石油资源和有效地减少汽车尾气的污染,还可以促进农业生产。乙醇(C2H5OH)完全燃烧的化学方程式为_______________,该反应属于____________(选填:“吸热”或“放热”)反应。
(4)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(5)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
CO2+ Ca(OH)2== CaCO3↓+ H2O Fe2O3+3CO2Fe+3CO2 高炉 C2H5OH+3O23H2O+2CO2 放热 2NaCl+ H2O2NaOH + H2↑+Cl2↑ BaCO3+2HCl == BaCl2+ H2O + CO2↑ 复分解反应 【解析】(1)石灰浆中含有较多未溶解的Ca(OH)2,能与空气中的二氧化碳反应生成坚硬的碳酸钙。(2)工业炼铁...查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:综合题
维生素C主要存在于蔬菜、水果中,其分子式为C6H8O6,在空气中易氧化变质.
(1)维生素C中C、H、O三种元素的质量比为____________(用最简比表示).
(2)为测定某鲜榨橙汁中维生素C的含量,兴趣小组进行如下实验:
步骤1 取橙汁样品,加入活性炭,振荡、静置、过滤,滤液移至小烧杯中,盖上玻璃片.
步骤2 配制碘(I2)溶液,测得其浓度为1.27g/L(即1升碘溶液中含有1.27克I2).
步骤3 快速移取20.00mL处理后的橙汁样品置于锥形瓶中,滴入碘溶液,恰好完全反应时消耗碘溶液10.00mL.(测定原理:C6H8O6+I2═C6H6O6+2HI)
①步骤1中活性炭的作用是__________________________.
②步骤3必须在步骤1、步骤2之后立即进行的原因是__________________________.
③计算1L该橙汁样品中含有维生素C的质量:______________g.(请写出计算过程)
9:1:12 活性炭可以吸附橙汁中的色素,便于观察后面反应中颜色的变化 维生素C在空气中易氧化变质,所以步骤3必须在步骤1,步骤2后立即进行 0.44 【解析】(1)维生素C中C、H、O三种元素的质量比为(12×6):(1×8):(16×6)=9:1:12 (2)①步骤1中活性炭的作用是可以吸附橙汁中的色素,便于观察后面反应中颜色的变化。 ②步骤3必须在步骤1、步骤2之后立即进行...查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:填空题
完成下列实验.(1)现提供下列装置:

①写出上图中B装置甲仪器的名称 .
②实验室用A装置进行高锰酸钾制氧气的实验,化学方程式为 ,用D装置收集氧气,气体由导管
进入(填“a”或“b”)
③实验室用锌粒和稀盐酸制氢气,用C装置代替B装置的优点是 :若要检验氧气中是否含有氯化氢气体,可将气体通过盛有 溶液的D装置(填“AgNO3”或“饱和NaHCO3溶液”)
(2)对一定质量的粗盐(含泥沙)进行初步提纯.
①实验主要步骤:称量与 、过滤、蒸发;实验中多次使用玻璃棒.过滤时它的作用是 ;蒸发时,待蒸发皿中出现 时停止加热.利用余热将滤液蒸干.
②下列因素会导致获得的精盐质量偏小的是 (填序号)
a.蒸发是液滴溅出 b.过滤时,滤纸破损
c.粗盐中加入过量的水 d.过滤后,滤纸上的泥沙未同水冲洗.
(1)分液漏斗; 2KMnO4K2MnO+MnO2+O2↑;a;节约药品;AgNO3;(2)溶解;引流;较多量晶体;ad 【解析】(1)①B装置甲仪器是分液漏斗;②高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的方程式是:2KMnO4K2MnO+MnO2+O2↑;氧气的密度比空气大,所以用装置D收集氧气时,氧气从长管进入;故填:③C装置与B装置比较可知,C装置容器小,节约药品;氯化氢溶于水形成...查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:流程题
实验室以MnO2为原料制备少量高纯MnCO3的流程如下:
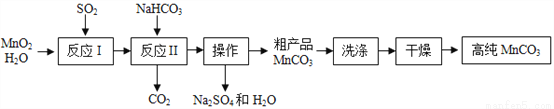
已知:①反应Ⅰ的化学方程式:MnO2+SO2═MnSO4;
②MnCO3、Mn(OH)2均难溶于水,MnCO3在100℃时开始分解.
(1)反应Ⅰ属于基本反应类型中的______________反应.
(2)流程中“操作”的名称为___________,所需要的主要玻璃仪器有__________.
(3)反应Ⅱ的化学方程式为_______________________.反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有______________(填化学式).
(4)验证MnCO3粗产品表面附着有Na2SO4杂质:取样品少许,向其中加入水,搅拌、过滤,向滤液中加入适量的______________(填化学式)溶液,有白色沉淀产生.
(5)为获得高纯MnCO3,需选择“低温”干燥的原因是_______________________.
化合 过滤 漏斗、玻璃棒、烧杯 MnSO4+2NaHCO3=Na2SO4+MnCO3↓+CO2↑+H2O Mn(OH)2 BaCl2 MnCO3的分解温度为100℃,为防止MnCO3高温分解,影响高纯MnCO3的纯度 【解析】(1)反应Ⅰ是MnO2+SO2═MnSO4,由两种物质发生化学反应生成一种物质的反应属于化合反应。(2)通过过滤可将固体与液体分离,过滤时用到的玻璃仪器有漏斗、玻璃棒、...查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:推断题
如图为某些物质间的转化关系.E为常见的碱,F常作食品干燥剂,M为石膏的主要成分.部分反应物和生成物已略去.

(1)化学式:C________,F_________.
(2)反应①、③的化学方程式:
①_____________________________________________,
③_____________________________________________.
(3)能体现明代《天工开物》中“煤饼烧石成灰”的反应是_____(选填反应序号).
(4)工业上可用B和H合成乙醇(C2H6O),反应中B和H的质量比为______.
H2O CaO Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 2Ca(OH)2+2SO2+O2=2CaSO4↓+2H2O ② 22:3 【解析】(1)E为常见的碱,F常作食品干燥剂,所以F是氧化钙,M为石膏的主要成分,所以M是硫酸钙,碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳,C通电会生成G和H,所以C是水,G、H是氢气和氧气中的一种,D会生成氧化钙和B,所以D是碳酸钙,B是二...查看答案和解析>>
科目: 来源:江苏省苏州市2018届九年级模拟化学测试卷(4) 题型:填空题
某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.
研究主题:水溶液中复分解反应的实质
相关信息:一定体积的溶液中,离子的数目越多,其离子的浓度越大.电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小.相同温度下同种溶液电导率越大,离子浓度越大.
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示.
①写出Ba(OH)2与H2SO4反应的化学方程式 .
②甲曲线M点时混合液体呈 色;
③通过对甲曲线的分析,下列说法错误的是 (填序号).
A.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4[
B.M点时离子浓度几乎为零 C.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示.
①通过对乙曲线的分析,下列说法错误的是 (填序号).
A.开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B.电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
C.整个实验过程中,溶液中Na+数目一直增大
②N点时,溶液中含有的离子是 (填离子符号).
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度 (填“增大”或“减小”).
(3)拓展:①请根据示例仿写离子方程式.
示例AgNO3+NaCl=AgCl↓+NaNO3离子方程式:Ag++Cl﹣=AgCl↓
仿写:BaCl2+Na2SO4=BaSO4↓+2NaCl离子方程式: .
②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊后浑浊逐渐消失.请推测此过程的溶液中Ca2+的浓度变化情况 .

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com