
科目: 来源: 题型:
【题目】(7分)已知某固体混合物中可能含有NH4Cl、Na2SO4、NH4NO3、CuO,所有发生的反应都恰好完全反应。根据实验过程和发生的现象填写以下空白:
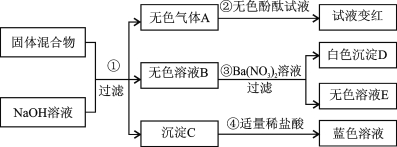
(1)气体A溶液的pH_______7。
(2)沉淀D的化学式为 。
(3)一定有的物质是 。
(4)该固体混合物中,还不能确定存在的是 ,(写化学式)要进一步推理该固体混合物的组成,可用溶液E再实验确定可能含有的物质:
实验操作 | 实验现象 | 实验结论 |
取未知成分溶液E少许,加入 溶液, | (用化学式表示) |
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米碳酸钙是一种重要的无机化工产品,下图是某厂生产纳米碳酸钙的工艺流程。

请回答下列问题:
(1)请完成并配平该工艺中生成CaCO3固体的反应方程式:
CaCl2 + ______ + CO2 ![]() CaCO3↓ + ______ + H2O
CaCO3↓ + ______ + H2O
(2)若在实验室中进行该实验,操作l的名称是 ,使用到的玻璃仪器有玻璃棒、_____、______,其中玻璃棒的作用是 。
(3)操作2为洗涤、干燥,其中洗涤的目的是除去碳酸钙粗品表面含有的可溶性杂质,其中一定含有的可溶性杂质是 ,检验是否洗涤干净的方法是向最后一次洗涤液中加入 溶液(①Ca(OH)2 、② AgNO3 、③CaCl2,填写序号),如果没有出现沉淀,说明已经洗涤干净。
(4)上述流程中的副产品(NH4Cl)可用作____________肥(填化肥种类)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组设计了测定纯碱(Na2CO3)样品(只含NaCl杂质)中Na2CO3质量分数的 实验方案.请回答下列问题:
小资料:碱石灰的主要成分是氢氧化钠和氧化钙的混合物
(1)气体法。
【原理思路】利用Na2CO3与稀硫酸反应产生CO2,通过测量丙装置实验前后的质量得出CO2质量,从而计算碳酸钠的质量分数。(不考虑原装置内空气的影响)
【实验分析】小科同学根据以上思路,设计了如图实验装置。

①实验装置乙中盛放的试剂为 ,其作用是 ;
装置丁中碱石灰的作用是 。(填字母)
A.吸收Na2CO3与稀硫酸反应产生CO2
B.防止外界空气中二氧化碳进入丙中
C.干燥二氧化碳
②实验中如果滴加稀硫酸的速度过快,会导致测得样品中碳酸钠的质量分数 (填写“偏高”、“偏低”或“不变”).
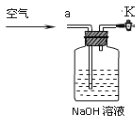
③小明同学认为小科的方案存在问题,不考虑原装置内空气的影响,即使操作规范,但由于生成的CO2在装置中残留,也会造成测得结果 (填写“偏高”、“偏低”或“不变”),应该将装置甲中双孔橡胶塞换成三孔橡胶塞,并增加下图装置,实验结束后缓缓通入一段时间空气,目的是 ,其中图中NaOH溶液的作用是 。
(2)沉淀法.
【实验原理】利用碳酸根离子与钙离子结合生成沉淀,通过沉淀的质量而得出碳酸钠的质量分数。
【实验步骤】①用托盘天平称取样品11.0g放入烧杯中,加水使其完全溶解;
②加入过量的CaCl2溶液充分反应。证明CaCl2过量(即让样品中Na2CO3完全反应)的方法是:静置,向上层清液中滴加 溶液,如果没有白色沉淀生成,证明CaCl2过量;
③过滤、洗涤、干燥、称量沉淀的质量为10.0g,由于沉淀表面粘附滤液,不经洗涤就烘干,称量沉淀的质量将会 (填写“偏高”、“偏低”或“不变”)。
④通过以上提供的数据计算出样品中碳酸钠的质量分数。(写出计算过程,结果保留至0.1%,共3分,只写出化学方程式给1分)
查看答案和解析>>
科目: 来源: 题型:
【题目】取实验室中部分变质的NaOH样品配成溶液,向其中滴加稀盐酸,绘制出生成的CO2的质量与加入的盐酸的质量关系如图所示,下列有关说法正确的是
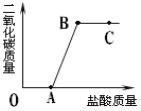
A.OA段没有发生任何化学反应
B.A点溶液中的溶质只有NaCl
C.B点表示加入的盐酸与原溶液中的溶质恰好完全反应
D.C点的溶液的pH=7
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是某保健品标签的部分内容,请仔细阅读后回答下列问题。

(1)该保健品的主要功能是 ,其主要成分中,提供钙元素的物质是 ;参与钙的代谢,促进其吸收的物质成分是 ;矿物质中的锌元素属于人体的 元素(选填“微量”或“常量”)。
(2)服用该保健品后,有时会出现腹胀、打嗝的反应,出现这种反应的原因是(化学方程式表示) 。
(3)每片中钙元素的质量是 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com