
| A. | 该氢燃料充电电池是将电能转化为化学能 | |
| B. | 固态金属合金作还原剂 | |
| C. | 该电池工作过程中的总反应为H2+M═MH2 | |
| D. | 该电池反应的最终产物为H2O |
分析 A、新型氧燃料充电电池是将化学能转化为电能的装置;
B、在反应中负极上是氢气失电子的氧化反应;
C、燃料电池的总反应是燃料燃烧的方程式;
D、燃料电池的总反应是燃料燃烧,据此确定反应产物.
解答 解:A、新型氧燃料充电电池是将化学能转化为电能的装置,故A错误;
B、在反应中负极上是氢失电子的氧化反应,故B错误;
C、燃料电池的负极上是氢气失电子的反应,正极上是氧气电子的反应,所以总反应是2H2+O2═2H2O,故C错误;
D、燃料电池的总反应是燃料燃烧,反应产物是水,故D正确.
故选D.
点评 本题考查学生燃料电池的工作原理以及电极反应式的书写知识,注意知识的归纳和梳理是关键,难度中等.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-4的溶液中:Na+、SiO32-、SO32-、K+ | |
| B. | 加入Al能放出H2的溶液中:Cl-、Mg2+、NO3-、K+ | |
| C. | 由水电离出的c(OH-)=10-13mol•L-1的溶液中:ClO-、Na+、SO32-、Cl- | |
| D. | pH=1的溶液中:Mg2+、Br-、K+、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L CO完全燃烧生成CO2分子数为NA | |
| B. | 17g 氨气所含电子数为NA | |
| C. | 在常温、常压下,11.2L氯气所含的原子数目为NA | |
| D. | 32g氧气所含的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| A | B | C | ||
| (1) | 1 | 3 | 0 | 放出热量a kJ |
| (2) | 0 | 0 | 2 | 吸收热量b kJ |
| (3) | 2 | 6 | 0 | 放出热量c kJ |
| A. | A的体积分数:(2)>(1)>(3) | |
| B. | 三个容器内反应的平衡常数:K(3)=K2(1)=K2(2) | |
| C. | 达平衡时体系压强:P(3)=2P(1) | |
| D. | 热量关系:a+b=50 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
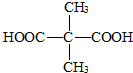 .
.
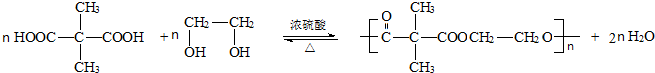 反应类型:缩聚反应.
反应类型:缩聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com