
| A. | 用N2和H2合成NH3 | B. | 闪电时大气中氮的氧化物的生成 | ||
| C. | 由氨制尿素 | D. | 从空气中分离出氮气 |
分析 氮的固定是指:将空气中游离态的氮转化为含氮化合物的过程.游离态是指氮气单质,人工固氮是人为的条件下将氮元素的单质转化为化合物的过程.
解答 解:A.工业上将N2合成氨,N2→NH3,氮气是单质,是游离态的氮,转变为化合态NH3,符合氮的固定定义,属于人工固氮,故A正确;
B.闪电时,氮气和氧气反应生成NO,属于自然固氮,故B错误;
C.用氨制尿素,是含氮化合物之间的相互转化,不符合氮的固定定义,故C错误;
D.从空气中分离出氮气的过程利用的是氮气和氧气沸点的不同,不是化学变化,不属于固氮,故D错误;
故选A.
点评 本题主要考查氮的固定,依据氮的固定是将空气中游离态的氮转化为含氮化合物的过程即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题

| A. | N为乙酸 | |
| B. | 过程①中可加入LiAlH4等还原剂将乙醇转化为N | |
| C. | 过程②如果加热一段时间后发现忘记加瓷片,应停止反应,待冷却后补加 | |
| D. | 可用饱和碳酸钠溶液除去乙酸乙酯中混有的N |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
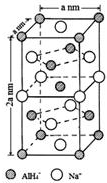 氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示. .
.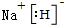 .
. (标明配位键).
(标明配位键).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ⑤⑥ | C. | ③④ | D. | ⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,增加反应物的量,必定加快反应速率 | |
| B. | 升高温度正反应速率增大,则逆反应速率也一定增大 | |
| C. | 可逆反应的特征是正反应速率总是和逆反应速率相等 | |
| D. | 使用催化剂一定会加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非极性分子中的原子一定无孤电子对 | |
| B. | 平面三角型分子一定是非极性分子 | |
| C. | 二氯甲烷(CH2Cl2)分子的中心原子是SP3杂化,键角均为109°28′ | |
| D. | ABn型分子的中心原子最外层满足8电子结构,则ABn不一定是非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、Cl2 | B. | CH3CH3、HCl | C. | CH≡CH、HCl | D. | CH2=CH2、HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com