
| A. | 降低温度,正反应速率减小、逆反应速率增大 | |
| B. | 增大c(A)、c(B),K增大 | |
| C. | 该反应的化学方程式为2E(g)+F(s)?A(g)+2B(g) | |
| D. | 该反应的焓变△H>0 |
分析 A.降低温度,正逆反应速率都减小;
B.化学平衡常数只与温度有关;
C.根据化学平衡常数知,F是气体且是反应物;
D.降低温度,F浓度增大,说明平衡向逆反应方向移动,降低温度平衡向放热反应方向移动,则正反应是吸热反应.
解答 解:A.降低温度,减少活化分子百分数,所以正逆反应速率都减小,故A错误;
B.化学平衡常数只与温度有关,温度不变化学平衡常数不变,与物质浓度无关,故B错误;
C.根据化学平衡常数知,F是气体且是反应物,其反应方程式为2E(g)+F(g)?A(g)+2B(g),故C错误;
D.降低温度,F浓度增大,说明平衡向逆反应方向移动,降低温度平衡向放热反应方向移动,则正反应是吸热反应,焓变大于0,故D正确;
故选D.
点评 本题考查化学平衡常数、化学反应速率影响因素、化学平衡影响因素等知识点,为高频考点,化学平衡常数只与温度有关,与物质浓度无关,易错选项是B.


科目:高中化学 来源: 题型:选择题
| A. | 以下离子可存在于能使酚酞变红的溶液中:Na+,Ba2+,NO3-,Cl- | |
| B. | 以下离子可存在于含有0.1mol•L-1 Fe3+的溶液中:K+,Mg2+,I-,SO42- | |
| C. | 用氯水作为水的消毒剂的原理为:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 纯碱用于清洁厨具是由于它溶于水呈碱性的缘故:HCO3-+H2O?OH-+H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐,其化学式为:FeSO4•(NH4)2SO4•6H2O.硫酸亚铁在空气中易被氧化,而形成摩尔盐后就稳定了.硫酸亚铁铵可由硫酸亚铁与硫酸铵等物质的量混合制得.三种盐的溶解度(单位为g/100g水)如表:下图是模拟工业制备硫酸亚铁铵晶体的实验装置.
硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐,其化学式为:FeSO4•(NH4)2SO4•6H2O.硫酸亚铁在空气中易被氧化,而形成摩尔盐后就稳定了.硫酸亚铁铵可由硫酸亚铁与硫酸铵等物质的量混合制得.三种盐的溶解度(单位为g/100g水)如表:下图是模拟工业制备硫酸亚铁铵晶体的实验装置.| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4•7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| 摩尔盐 | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥⑦⑧ | B. | ①④⑥⑦⑧ | C. | ①⑧ | D. | ①④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
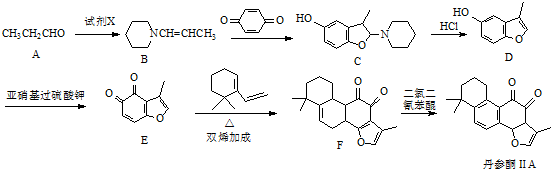
 .
. .
. 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com