
科目: 来源: 题型:
下列叙述中,正确的是:
A.钢铁腐蚀的负极反应为:Fe-3e- = Fe3+
B.Mg—Al及NaOH溶液构成的原电池中负极材料为Mg
C.甲烷燃料电池的正极反应为:O2+2H2O+4e-=4OH-
D.乙醇燃料电池的电解质常用KOH,该电池的负极反应为:
C2H5OH-12e-=2CO2↑+3H2O
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是:
A.烧碱溶液中加入铝片:Al + OH- + H2O= AlO![]() +H2↑
+H2↑
B.苯酚钠溶液中通入少量CO2:C6H5O-+CO2+H2O = C6H5OH + HCO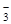
C.澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO![]() =CaCO3↓+CO
=CaCO3↓+CO![]() +2H2O
+2H2O
D.硝酸亚铁溶液中滴加盐酸:3Fe2++4H++NO![]() =3Fe3++2H2O+NO↑
=3Fe3++2H2O+NO↑
查看答案和解析>>
科目: 来源: 题型:
除去下列物质中所含少量杂质的方法正确的是:
|
| 物 质 | 杂 质 | 试 剂 | 提 纯 方 法 |
| A | BaSO4 | BaCO3 | 稀盐酸 | 溶解、过滤、洗涤 |
| B | CO2 | SO2 | 饱和Na2CO3溶液 | 洗气 |
| C | 乙酸乙酯 | 乙酸 | 稀NaOH溶液 | 混合振荡、静置分液 |
| D | 蛋白质 | 蔗糖 | 浓(NH4)2SO4溶液 | 盐析、过滤、洗涤 |
查看答案和解析>>
科目: 来源: 题型:
由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用的塑料。
(1)聚合物F的结构简式是_____________________________________。
(2)D的结构简式是___________________________________________。
(3)B转化为C的化学方程式是_________________________。
(4)在一定条件下,两分子E能脱去两分子水形成一种六元环化合物,该化合物的结构简式是______________________。
(5)E有多种同分异构体,其中一种能发生银镜反应,1mol该种同分异构体与足量的金属钠反应产生1mol H2,则该种同分异构体为__________________________。
查看答案和解析>>
科目: 来源: 题型:
锌钡白是BaSO4和ZnS的混合物,ZnS难溶于水。某化工厂用重晶石为原料制备锌钡白,生产过程中会产生大量废气(主要成分为CO2、CO及少量SO2和硫蒸气等),为防止污染空气并提高原料利用率,生产中采用下述工艺流程:
请根据上述流程回答下列问题:
(1)重晶石的化学式为_________,锌钡白可用于调制_______色和浅色油漆。
(2)处理过程(a)的步骤为:①_____________;②洗涤;③______________。
(3)设备1是冷却分离塔,若设备1前面的导气管过长、过窄,可能使导气管堵塞,其原因是 。
(4)设备2中所用的洗涤剂是NaOH溶液,则y的化学式为 。写出设备2中发生反应的离子方程式:_____________________、_____________。
(5)可用 法分离溶液中的钠盐,进行分离前,需要查得的是
。(数据)
(6)制备过程中得到的硫磺,除了可用来制硫酸外,其它的用途为 (至少写一种)。
查看答案和解析>>
科目: 来源: 题型:
在80℃时,0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)计算20s~40s内用N2O4表示的平均反应速率为 。
(2)计算在80℃时该反应的平衡常数K 。
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色 (填“变浅”、“变深”或“不变”)。
(4)要增大该反应的K值,可采取的措施有(填序号) ,若要重新达到平衡时,使[NO2]/[N2O4]值变小,可采取的措施有(填序号) 。
A.增大N2O4的起始浓度 B.向混合气体中通入NO2
C.使用高效催化剂 D.升高温度
(5)如右图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线。
查看答案和解析>>
科目: 来源: 题型:
甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
(1)甲组:沉淀分析法:
把一定量的混合物溶解后加入过量CaCl2,然后将所得沉淀过滤、洗涤、烘干、称量。确定CaCl2溶液是否过量的方法是 洗涤沉淀并判断沉淀是否洗净的操作是_______________________________________。
(2)乙组:气体分析法:
把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是____________,选用该溶液后实验结果还是不准确,原因是_________________。
(3)请你设计一个与甲、乙两组操作不同的实验方案,测定混合
物中Na2CO3的含量。
方法: ;
试剂:_________________________________________________________________。
用到的玻璃仪器:_______________________________________________(至少2件)。
查看答案和解析>>
科目: 来源: 题型:
在溶液中能大量共存的一组离子或分子是
A.NH4+、H+、NO3-、HCO3- B.K+、Al3+、SO42-、NH3·H2O
C.Na+、K+、SO32-、Cl2 D.Na+ 、CH3COO-、CO32-、OH-
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏伽德罗常数,下列叙述正确的是
A.24g镁原子最外层电子数为NA
B.1L0.1mol·L-1乙酸溶液中H+数为0.1NA
C.1mol甲烷分子所含质子数为10NA
D.标准状况下,22.4L乙醇的分子数为NA
查看答案和解析>>
科目: 来源: 题型:
已知:Fe2O3 (s)+C(s)= CO2(g)+2Fe(s) △H=234.1kJ·mol-1
C(s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1 则2Fe(s)+O2(g ) = Fe2O3(s)的△H是
A.-824.4kJ·mol-1 B.-627.6kJ·mol-1
C.-744.7kJ·mol-1 D.-169.4kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com