
题目列表(包括答案和解析)
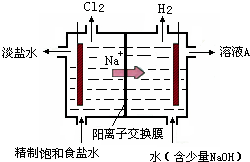
 氯碱工业中电解饱和食盐水的原理示意图如图所示:
氯碱工业中电解饱和食盐水的原理示意图如图所示:
氯碱工业中电解饱和食盐水的原理示意图如右图所示。
⑴溶液A的溶质是 。
⑵电解饱和食盐水的离子方程式是 。
 ⑶电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用: 。
⑶电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用: 。
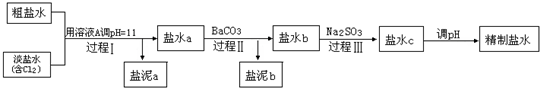
⑷电解所用的盐水需精制,去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42-)>c(Ca2+)]。精制流程如下(淡盐水和溶液A来自电解池):

①盐泥a除泥沙外,还含有的物质是 。
②过程I中将NH4+转化为N2的离子方程式是 。
③BaSO4的溶解度比BaCO3的小。过程II中除去的离子有 。
④经过程III处理,要求盐水c中剩余Na2SO3的含量小于5mg/L。若盐水b中NaClO的含量是7.45mg/L,则处理10m3盐水b,至多添加10% Na2SO3溶液 kg(溶液体积变化忽略不计)。
(8分)氯碱工业中电解饱和食盐水的原理示意图如图所示:
(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是 ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用 ;
(4)检验阳极反应产物的方法是:______________________________________________________
___________________________________________________________________________________
(12分)氯碱工业中电解饱和食盐水的原理示意图如下图所示:
(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是 ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用 ;
(4)电解所用的盐水需精制。去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42-)>c(Ca2+)]。
精致流程如下(淡盐水和溶液A来自电解池):
①盐泥a除泥沙外,还含有的物质是 。
②过程Ⅰ中将NH4+转化为N2的离子方程式是
③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有
④经过程Ⅲ处理,要求盐水中c 中剩余Na2SO3的含量小于5mg /L,若盐水b中NaClO的含量是7.45 mg /L ,则处理10m3 盐水b ,至多添加10% Na2SO3溶液 kg(溶液体积变化忽略不计)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com