
题目列表(包括答案和解析)
工业废水中常含有一定量的 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为

其中第①步存在平衡:

(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr O
O
 和CrO
和CrO 的浓度相同
的浓度相同
b.2v (Cr O
O ) =v (CrO
) =v (CrO )
)
c.溶液的颜色不变
(3)第②步中,还原1mol Cr O
O 离子,需要 mol的FeSO
离子,需要 mol的FeSO ·7H
·7H O。
O。
(4)第③步生成的Cr(OH) 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:

常温下,Cr(OH) 的溶度积
的溶度积 ,要使c(Cr3+)降至10
,要使c(Cr3+)降至10 mol/L,溶液的pH应调至
。
mol/L,溶液的pH应调至
。
方法2:电解法
该法用Fe做电极电解含Cr O
O 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH) 沉淀。
沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
溶液中同时生成的沉淀还有 。
工业废水中常含有一定量的,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
其中第①步存在平衡:
(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr![]() O
O![]()
![]() 和CrO
和CrO 的浓度相同
的浓度相同
b.2v (Cr O
O![]() ) =v (CrO
) =v (CrO![]() )
)
c.溶液的颜色不变
(3)第②步中,还原1mol Cr![]() O
O![]() 离子,需要 mol的FeSO
离子,需要 mol的FeSO![]() ·7H
·7H![]() O。
O。
(4)第③步生成的Cr(OH)![]() 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:
常温下,Cr(OH)![]() 的溶度积
的溶度积,要使c(Cr3+)降至10
![]() mol/L,溶液的pH应调至 。
mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr![]() O
O![]() 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)![]() 沉淀。
沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
溶液中同时生成的沉淀还有 。
工业废水中常含有一定量的 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为 
其中第①步存在平衡: 
(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr O
O
 和CrO
和CrO 的浓度相同
的浓度相同
b.2v (Cr O
O ) ="v" (CrO
) ="v" (CrO )
)
c.溶液的颜色不变
(3)第②步中,还原1mol Cr O
O 离子,需要 mol的FeSO
离子,需要 mol的FeSO ·7H
·7H O。
O。
(4)第③步生成的Cr(OH) 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:
常温下,Cr(OH) 的溶度积
的溶度积 ,要使c(Cr3+)降至10
,要使c(Cr3+)降至10 mol/L,溶液的pH应调至 。
mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr O
O 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH) 沉淀。
沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
溶液中同时生成的沉淀还有 。
 ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。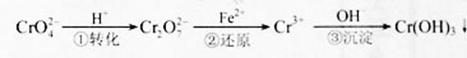

 O
O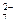
 和CrO
和CrO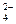 的浓度相同
的浓度相同 O
O ) ="v" (CrO
) ="v" (CrO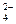 )
) O
O 离子,需要 mol的FeSO
离子,需要 mol的FeSO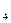 ·7H
·7H O。
O。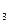 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:
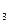 的溶度积
的溶度积 ,要使c(Cr3+)降至10
,要使c(Cr3+)降至10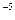 mol/L,溶液的pH应调至 。
mol/L,溶液的pH应调至 。 O
O 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH) 沉淀。
沉淀。| H+ |
| ①转化 |
| Fe2+ |
| ②还原 |
| OH- |
| ③沉淀 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com