
题目列表(包括答案和解析)
(注意:在试题卷上作答无效)
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,在将滤液按下图所示步骤进行操作。
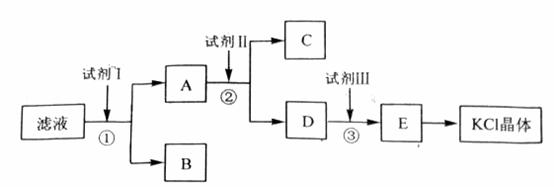
回答下列问题:
(1) 起始滤液的pH_____________7(填“大于”、“小于”或“等于”),其原因是_________________________________________________。
(2) 试剂I的化学式为______________________,①中发生反应的离子方程式为____________________________________________。
(3) 试剂Ⅱ的化学式为______________________,②中加入试剂Ⅱ的目的是__________________________________________________________________;
(4) 试剂Ⅲ的名称是______________________,③中发生反应的离子方程式为__________________________________________________________________;
(5) 某同学称取提纯的产品0.7759g,溶解后定定容在100mL容量瓶中,每次取25.00mL溶液,用0.1000mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62mL,该产品的纯度为____________________________________________。(列式并计算结果)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com