研究NO
2、SO
2、CO等大气污染气体的处理具有重要意义.

(1)利用反应6NO
2+8NH
37N
2+12H
2O可以处理NO
2.当转移1.2mol电子时,生成的N
2在标准状况下是
7.84
7.84
L.
(2)已知:2SO
2(g)+O
2(g)?2SO
3(g)△H=-196.6kJ?mol
-1 2NO(g)+O
2(g)?2NO
2(g)△H=-113.0kJ?mol
-1则反应NO
2(g)+SO
2(g)?SO
3(g)+NO(g)的△H=
-41.8
-41.8
kJ?mol
-1.一定条件下,将NO
2与SO
2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
b
b
.
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO
3和NO的体积比保持不变
d.每消耗1mol SO
3的同时生成1mol NO
2测得上述反应平衡时NO
2与SO
2体积比为1:6,则平衡常数K=
2.67
2.67
.
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H
2(g)?CH
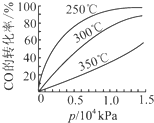
3OH(g).CO在不同温度下的平衡转化率与压强的关系如图1所示.该反应△H
<
<
0(填“>”或“<”).实际生产条件控制在250℃、1.3×10
4kPa左右,选择此压强的理由是
在1.3×104kPa下,CO的转化率已较高,若再增大压强,CO的转化率提高不大,且生产成本增加,得不偿失
在1.3×104kPa下,CO的转化率已较高,若再增大压强,CO的转化率提高不大,且生产成本增加,得不偿失
.
(4)某实验小组依据甲醇燃烧的反应原理,设计如图2所示的装置.已知甲池的总反应式为:2CH
3OH+3O
2+4KOH═2K
2CO
3+6H
2O.请回答:
①通入O
2的电极名称是
正
正
,B电极的名称是
阳
阳
.
②通入CH
3OH的电极的电极反应式是
CH3OH+8OH-+6e-=CO32-+6H2O
CH3OH+8OH-+6e-=CO32-+6H2O
,A电极的电极反应式为
Ag++e-=Ag
Ag++e-=Ag
.

 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
