
题目列表(包括答案和解析)
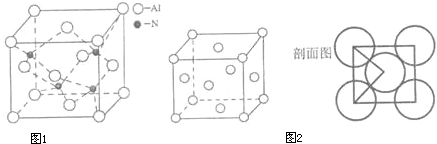

【化学—物质结构与性质】
氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为______个。
(2)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为______________________________。
HO―![]() ―CHO的沸点比
―CHO的沸点比![]() 高,原因是______________________________。
高,原因是______________________________。
(3) H+可与H2O形成H3O+,H3O+中O原子采用_________杂化。H3O+中H-O-H键角比H2O中H-O-H键角大,原因为____________________________________。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为a g•cm-3,NA表示阿伏伽德罗常数,则CaO晶胞体积为________cm3。

磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)="==" 6CaO(s)+P4(s)+10CO(g) △H1 ="+3359.26" kJ·mol-1
CaO(s)+SiO2(s)="==" CaSiO3(s) △H2 ="-89." 61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)="==" 6CaSiO3(s)+P4(s)+10CO(g) △H3
则△H3 = kJ·mol-1。
(2)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示:
11P 4+60CuSO4+96H2O="==" 20Cu3P+24H3PO4+60H2SO4
60molCuSO4能氧化白磷的物质的量是 。
(3)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示。
①为获得尽可能纯的NaH2PO4,pH应控制在 ;pH=8时,溶液中主要含磷物种浓度大小关系为 。
②Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是
(用离子方程式表示)。
(4)磷的化合物三氯氧磷(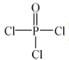 )与季戊四醇(
)与季戊四醇( )以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X 的核磁共振氢谱如下图所示。
)以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X 的核磁共振氢谱如下图所示。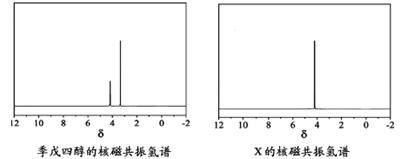
①酸性气体是 (填化学式)。
②X的结构简式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com