
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
Ђё.дкЬхЛ§КуЖЈЕФУмБеШнЦїжаЃЌГфШы2mol CO2КЭ5mol H2ЃЌвЛЖЈЬѕМўЯТЗЂЩњЗДгІЃК CO2(g) + 3H2(g)  CH3OH(g)
+ H2O(g) ЁїH = -49.0 kJ/molЁЃВтЕУCO2КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЃК
CH3OH(g)
+ H2O(g) ЁїH = -49.0 kJ/molЁЃВтЕУCO2КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЃК

ЃЈ1ЃЉДгЗДгІПЊЪМЕНЕк10minЃЌH2ЕФзЊЛЏТЪЮЊ ЃЌдк ИУЬѕМўЯТЃЌЗДгІЕФЦНКтГЃЪ§K= ЃЌШчЙћдкФГвЛЪБПЬБЃГжЮТЖШВЛБфЃЌжЛИФБфХЈЖШЃЌЪЙc(CO2)=1.00mol/LЃЌc(H2)=0.40mol/LЃЌc(CH3OH)=c(H2O)=0.80mol/LЃЌдђЦНКт ЃЈбЁЬюађКХЃЉЁЃ
aЃЎЯђе§ЯђвЦЖЏ bЃЎЯђФцЯђвЦЖЏ
cЃЎВЛвЦЖЏ dЃЎЮоЗЈШЗЖЈЦНКтвЦЖЏЗНЯђ
ЃЈ2ЃЉЯТСаДыЪЉжаФмЪЙn(CH3OH)/n(CO2)діДѓЕФЪЧ ЃЈбЁЬюађКХЃЉЁЃ
aЃЎЩ§ИпЮТЖШ bЃЎГфШыHe(g)ЃЌЪЙЬхЯЕбЙЧПдіДѓ
cЃЎНЋH2O(g)ДгЬхЯЕжаЗжРы dЃЎдйГфШыl mol CH3OH(g)
IIЃЎШлШкЬМЫсбЮШМСЯЕчГиЃЈMCFSЃЉЃЌЗЂУїгк1889ФъЁЃЯжгавЛИіЬМЫсбЮШМСЯЕчГиЃЌвдвЛЖЈБШР§Li2CO3КЭNa2CO3ЕЭШлЛьКЯЮяЮЊЕчНтжЪЃЌВйзїЮТЖШЮЊ650ЁцЃЌдкДЫЮТЖШЯТвдФјЮЊДпЛЏМСЃЌвдУКЦјЃЈCOЁЂH2ЕФЬхЛ§БШЮЊ1:1ЃЉжБНгзїШМСЯЃЌЦфЙЄзїдРэШчЭМЫљЪОЁЃЧыЛиД№ЯТСаЮЪЬтЃК

ЃЈ1ЃЉAЕчМЋЕФЕчМЋЗДгІЗНГЬЪНЮЊ ЁЃ
ЃЈ2ЃЉГЃЮТЯТЃЌгУЪЏФЋзїЕчМЋЃЌвдДЫЕчдДЕчНтвЛЖЈСПЕФCuSO4 ШмвКЁЃЕБСНМЋВњЩњЕФЦјЬхЬхЛ§ЯрЭЌЪБЭЃжЙЭЈЕчЃЌШєЕчНтКѓШмвКЕФЬхЛ§ЮЊ2LЃЌШмвКЕФpH=1ЃЈВЛПМТЧЫЎНтВњЩњЕФH+ЃЉЃЌдђбєМЋВњЩњЕФЦјЬхЕФЮяжЪЕФСПЪЧ ЁЃ
Ђё.дкЬхЛ§КуЖЈЕФУмБеШнЦїжаЃЌГфШы2mol CO2КЭ5mol H2ЃЌвЛЖЈЬѕМўЯТЗЂЩњЗДгІЃК CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ЁїH =" -49.0" kJ/molЁЃВтЕУCO2КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЃК
CH3OH(g) + H2O(g) ЁїH =" -49.0" kJ/molЁЃВтЕУCO2КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЃК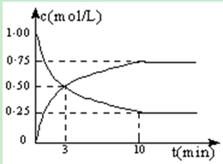
ЃЈ1ЃЉДгЗДгІПЊЪМЕНЕк10minЃЌH2ЕФзЊЛЏТЪЮЊ ЃЌдк ИУЬѕМўЯТЃЌЗДгІЕФЦНКтГЃЪ§K= ЃЌШчЙћдкФГвЛЪБПЬБЃГжЮТЖШВЛБфЃЌжЛИФБфХЈЖШЃЌЪЙc(CO2)=1.00mol/LЃЌc(H2)=0.40mol/LЃЌc(CH3OH)=c(H2O)=0.80mol/LЃЌдђЦНКт ЃЈбЁЬюађКХЃЉЁЃ
aЃЎЯђе§ЯђвЦЖЏ bЃЎЯђФцЯђвЦЖЏ
cЃЎВЛвЦЖЏ dЃЎЮоЗЈШЗЖЈЦНКтвЦЖЏЗНЯђ
ЃЈ2ЃЉЯТСаДыЪЉжаФмЪЙn(CH3OH)/n(CO2)діДѓЕФЪЧ ЃЈбЁЬюађКХЃЉЁЃ
aЃЎЩ§ИпЮТЖШ bЃЎГфШыHe(g)ЃЌЪЙЬхЯЕбЙЧПдіДѓ
cЃЎНЋH2O(g)ДгЬхЯЕжаЗжРы dЃЎдйГфШыl mol CH3OH(g)
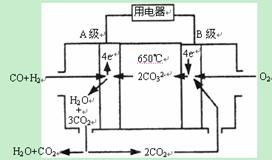
IIЃЎШлШкЬМЫсбЮШМСЯЕчГиЃЈMCFSЃЉЃЌЗЂУїгк1889ФъЁЃЯжгавЛИіЬМЫсбЮШМСЯЕчГиЃЌвдвЛЖЈБШР§Li2CO3КЭNa2CO3ЕЭШлЛьКЯЮяЮЊЕчНтжЪЃЌВйзїЮТЖШЮЊ650ЁцЃЌдкДЫЮТЖШЯТвдФјЮЊДпЛЏМСЃЌвдУКЦјЃЈCOЁЂH2ЕФЬхЛ§БШЮЊ1:1ЃЉжБНгзїШМСЯЃЌЦфЙЄзїдРэШчЭМЫљЪОЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉAЕчМЋЕФЕчМЋЗДгІЗНГЬЪНЮЊ ЁЃ
ЃЈ2ЃЉГЃЮТЯТЃЌгУЪЏФЋзїЕчМЋЃЌвдДЫЕчдДЕчНтвЛЖЈСПЕФCuSO4 ШмвКЁЃЕБСНМЋВњЩњЕФЦјЬхЬхЛ§ЯрЭЌЪБЭЃжЙЭЈЕчЃЌШєЕчНтКѓШмвКЕФЬхЛ§ЮЊ2LЃЌШмвКЕФpH=1ЃЈВЛПМТЧЫЎНтВњЩњЕФH+ЃЉЃЌдђбєМЋВњЩњЕФЦјЬхЕФЮяжЪЕФСПЪЧ ЁЃ
 CH3OH(g) + H2O(g) ЁїH =" -49.0" kJ/molЁЃВтЕУCO2КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЃК
CH3OH(g) + H2O(g) ЁїH =" -49.0" kJ/molЁЃВтЕУCO2КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЃК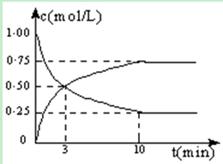
дкУмБеШнЦїжаЃЌНјааЯТСаЗДгІЃК (е§ЗДгІЮЊЮќШШЗДгІ)ДяЕНЦНКтКѓЃЌЯТСаЫЕЗЈжае§ШЗЕФЪЧ
(е§ЗДгІЮЊЮќШШЗДгІ)ДяЕНЦНКтКѓЃЌЯТСаЫЕЗЈжае§ШЗЕФЪЧ
[ЁЁЁЁ]
AЃЎШєКуЮТЖЈШнЧщПіЯТЃЌГфШывЛаЉЯЁгаЦјЬхЃЌбЙЧПдіДѓЃЌЕЋЦНКтВЛвЦЖЏ
BЃЎШєКуЮТЖЈбЙЬѕМўЯТЃЌМгШыC(g)ЃЌдђCЕФзЊЛЏТЪНЋдіДѓ
CЃЎШєЖЈШнЩ§ЮТЃЌдкаТЦНКтЬхЯЕжаAЕФжЪСПЗжЪ§НЋМѕаЁ
DЃЎЮТЖШЁЂбЙЧПКЭШнЛ§ЖМЯрЭЌЪБЃЌдкСэвЛУмБеШнЦїжаМгШы2molЁЁAЁЂ1molЁЁBЁЂ1molЁЁCЃЌЦНКтЪБСНИіШнЦїжаDКЭEЕФХЈЖШЗжБ№ЯрЕШ
дкУмБеШнЦїжаЃЌНјааЯТСаЗДгІЃК2A(g)ЃЋB(g)ЃЋC(s)![]() D(g)ЃЋE(g)(е§ЗДгІЮќШШ)ЃЌДяЕНЦНКтКѓЃЌЯТСаЫЕЗЈжае§ШЗЕФЪЧ
D(g)ЃЋE(g)(е§ЗДгІЮќШШ)ЃЌДяЕНЦНКтКѓЃЌЯТСаЫЕЗЈжае§ШЗЕФЪЧ
[ЁЁЁЁ]
AЃЎШєКуЮТЖЈШнЧщПіЯТЃЌГфШывЛаЉЯЁгаЦјЬхбЙЧПдіДѓЃЌЕЋЦНКтВЛвЦЖЏ
BЃЎШєКуЮТЖЈбЙЬѕМўЯТЃЌМгШыCЃЌдђBЕФзЊЛЏТЪНЋдіДѓ
CЃЎШєЖЈШнЩ§ЮТЃЌдкаТЦНКтЬхЯЕжаAЕФжЪСПЗжЪ§НЋМѕаЁ
DЃЎдкЮТЖШЁЂбЙЧПКЭШнЛ§ЖМЯрЭЌЪБЃЌдкСэвЛУмБеШнЦїжаМгШы2 mol AЃЌ1 mol BЃЌ1 mol CЃЌЦНКтЪБСНИіШнЦїжаDКЭEЕФХЈЖШЗжБ№ЯрЕШ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com