
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
¡°ÇâÄÜ¡±½«ÊÇδÀ´×îÀíÏëµÄĐÂÄÜÔ´¡£
¢ñ.ʵÑé²âµĂ£¬1gÇâÆøȼÉƠÉú³É̉º̀¬Ë®Ê±·Å³ö142.9kJÈÈÁ¿£¬ỘÇâÆøȼÉƠµÄÈÈ»¯Ñ§·½³̀ʽΪ_______¡££῭îĐ̣ºÅ£©
A.2H2£¨g£©+O2£¨g£©  2H2O£¨l£©
¡÷H= £142.9kJ¡¤mol¡ª1
2H2O£¨l£©
¡÷H= £142.9kJ¡¤mol¡ª1
B.H2£¨g£©+1/2 O2£¨g£©  H2O£¨l£©
¡÷H= £285.8kJ¡¤mol¡ª1
H2O£¨l£©
¡÷H= £285.8kJ¡¤mol¡ª1
C.2H2+O2 2H2O£¨l£©
¡÷H= £571.6kJ¡¤mol¡ª1
2H2O£¨l£©
¡÷H= £571.6kJ¡¤mol¡ª1
D.H2£¨g£©+1/2
O2£¨g£©  H2O£¨g£© ¡÷H= £285.8kJ¡¤mol¡ª1
H2O£¨g£© ¡÷H= £285.8kJ¡¤mol¡ª1
¢̣.ij»¯Ñ§¼̉¸ù¾Ư¡°Ô×Ó¾¼Ă¡±µÄ˼Ï룬Éè¼ÆÁËÈçÏÂÖƱ¸H2µÄ·´Ó¦²½Öè
¢ÙCaBr2+H2O CaO+2HBr ¢Ú2HBr+Hg
CaO+2HBr ¢Ú2HBr+Hg HgBr2+H2
HgBr2+H2
¢ÛHgBr2+_____ ______________
¢Ü2HgO
______________
¢Ü2HgO 2Hg+O2¡ü
2Hg+O2¡ü
ÇëÄă¸ù¾Ư¡°Ô×Ó¾¼Ă¡±µÄ˼ÏëÍê³ÉÉÏÊö²½Öè¢ÛµÄ»¯Ñ§·½³̀ʽ£º____________¡£
¸ù¾Ư¡°ẦÉ«»¯Ñ§¡±µÄ˼ÏëÆÀ¹À¸Ă·½·¨ÖÆH2µÄÖ÷̉ªÈ±µă£º______________¡£
¢ó.ÀûÓĂºËÄÜ°ÑË®·Ö½âÖÆÇâÆø£¬ÊÇÄ¿Ç°ƠưÔÚÑĐ¾¿µÄ¿Î̀â¡£ÏÂͼÊÇÆäÖеÄ̉»ÖÖÁ÷³̀£¬ÆäÖĐÓĂÁ˹ưÁ¿µÄµâ¡££῭áʾ£º·´Ó¦¢ÚµÄ²úÎïÊÇO2¡¢SO2ºÍH2O£©

Íê³ÉÏÂÁĐ·´Ó¦µÄ»¯Ñ§·½³̀ʽ£º
·´Ó¦¢Ù__________________________£»·´Ó¦¢Ú__________________________¡£
´Ë·¨ÖÆÈ¡ÇâÆøµÄ×î´óÓŵăÊÇ_______________________________________________¡£
¢ô.ÇâÆøͨ³£ÓĂÉú²úË®ĂºÆøµÄ·½·¨ÖÆµĂ¡£ÆäÖĐCO£¨g£©+ H2O£¨g£© 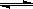 CO2£¨g£©+ H2£¨g£©; ¡÷H<0¡£
CO2£¨g£©+ H2£¨g£©; ¡÷H<0¡£
ÔÚ850¡æʱ£¬K=1¡£
£¨1£©ÈôÉư¸ßζȵ½950¡æʱ£¬´ïµ½Æ½ºâʱK______1£῭î¡°´óÓÚ¡±¡¢¡°Đ¡ÓÚ¡±»̣¡°µÈÓÚ¡±£©
£¨2£©850¡æʱ£¬ÈôỊ̈̉»ÈƯ»ư¿É±äµÄĂܱƠÈƯÆ÷ÖĐͬʱ³äÈë 1.0 mol CO¡¢3.0molH2O¡¢1.0mol CO2 ºÍ x mol H2£¬Ộ£º
¢Ùµ±x=5.0ʱ£¬ÉÏÊöƽºâỊ̈___________£῭îƠư·´Ó¦»̣Äæ·´Ó¦£©·½Ị̈½øĐĐ¡£
¢ÚÈổªÊ¹ÉÏÊö·´Ó¦¿ªÊ¼Ê±Ị̈Ơư·´Ó¦·½Ị̈½øĐĐ£¬ỘxÓ¦Âú×ăµÄ̀ơ¼₫ÊÇ__________¡£
£¨3£©ÔÚ850¡æʱ£¬ÈôÉèx£½5.0 molºÍx£½6.0mol£¬ÆäËüÎïÖʵÄͶÁϲ»±ä£¬µ±ÉÏÊö·´Ó¦´ïµ½Æ½ºâºó£¬²âµĂH2µÄ̀å»ư·ÖÊư·Ö±đΪa£¥¡¢b£¥£¬Ộa _______ b£῭î¡°´óÓÚ¡±¡¢¡°Đ¡ÓÚ¡±»̣¡°µÈÓÚ¡±£©¡£
¢ơ.ÇâÆø»¹ÔÑơ»¯ÍËùµĂµÄº́É«¹̀̀å¿ÉÄÜÊÇÍÓëÑơ»¯ÑÇ͵Ļ́ºÏÎ̉ÑÖªCu2OÔÚËáĐÔÈÜ̉ºÖĐ¿É·¢Éú×ÔÉíÑơ»¯»¹Ô·´Ó¦£¬Éú³ÉCu2+ºÍµ¥ÖÊÍ¡£
£¨1£©ÏÖÓĐ8¿ËÑơ»¯Í±»ÇâÆø»¹Ôºó£¬µĂµ½º́É«¹̀̀å6.8¿Ë£¬ÆäÖĐº¬µ¥ÖÊÍÓëÑơ»¯ÑÇ͵ÄÎïÖʵÄÁ¿Ö®±ÈÊÇ £»
£¨2£©Èô½«6.8¿ËÉÏÊö»́ºÏÎïÓë×ăÁ¿µÄÏ¡Ạ́Ëá³ä·Ö·´Ó¦ºó¹ưÂË£¬¿ÉµĂµ½¹̀̀å g£»
£¨3£©Èô½«6.8¿ËÉÏÊö»́ºÏÎïÓë̉»¶¨Á¿µÄŨÏơËá³ä·Ö·´Ó¦£¬
¢ÙÉú³É±ê×¼×´¿öÏÂ1.568ÉưµÄÆø̀壨²»¿¼ÂÇNO2µÄÈܽ⣬̉²²»¿¼ÂÇNO2ÓëN2O4µÄת»¯£©£¬Ộ¸ĂÆø̀åµÄ³É·ÖÊÇ £¬ÆäÎïÖʵÄÁ¿Ö®±ÈÊÇ £»
¢Ú°ÑµĂµ½µÄÈÜ̉ºĐ¡ĐÄƠô·¢Å¨Ëơ£¬°ÑÎö³öµÄ¾§̀å¹ưÂË£¬µĂ¾§̀å23.68g¡£¾·ÖÎö£¬ÔÈÜ̉ºÖеÄCu2+ÓĐ20%²ĐÁôÔÚĸ̉ºÖĐ¡£ÇóËùµĂ¾§̀åµÄ»¯Ñ§Ê½
 ¼ơÉÙNO2¡¢SO2¡¢COµÈÓĐº¦Æø̀å¶Ô´óÆø»·¾³µÄΣº¦£¬ÊÇÈËÀàµÄ¹²Í¬×·Çó£®
¼ơÉÙNO2¡¢SO2¡¢COµÈÓĐº¦Æø̀å¶Ô´óÆø»·¾³µÄΣº¦£¬ÊÇÈËÀàµÄ¹²Í¬×·Çó£®
| ||
| ¼Óѹ |
| ||
| ¼Óѹ |
| 3 |
| 2 |
| 3 |
| 2 |
| 8 |
| 3 |
| 8 |
| 3 |
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com