
题目列表(包括答案和解析)
| 二氧化锰 |
| 二氧化锰 |
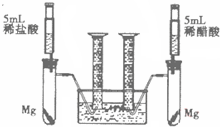 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.

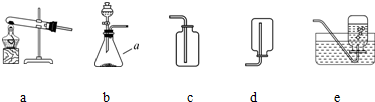
某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从下图中选择装置进行了氧气的制备实验.
(1)写出仪器a的名称: .
(2)甲同学从上图中选择B、E装置的组合制取氧气,反应的化学方程式为: .在用脚皮管连接装置B和E中的玻璃导管时,应先把玻璃管口 ,然后稍稍用力把玻璃管插入胶皮管.收集气体前,应将集气瓶装满 并盖上 .收集氧气还可选用的装置是 .
(3)乙同学称取一定质量的KMnO4固体放入大试管中,将温度控制在250℃加热制取O2.实验结束时,乙同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
[提出猜想]
猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2;
猜想Ⅲ:反应生成的K2MnO4和MnO2分解放出O2.
[实验验证]同学们分成两组,分别进行下列实验:第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变,则猜测 错误;第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是 .
[拓展延伸]实验发现,KClO3固体加热制取O2的反应速率很慢,但如果将KMnO4固体与KClO3固体混合加热,则KClO3的分解速率大大加快,请说明KMnO4在KClO3的分解反应中是否作催化剂,为什么? .
[实验反思]通过以上实验探究,你对“实验制取氧气”还想探究的问题是 .
 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.


| 实验操作 | 主要实验现象 | 实验结论和解释 |
| 另取样于试管加入过量的CaCl2溶液,静置后,取上层清液,滴入酚酞试液 | ①______; ②______; | 该溶液是变质的NaOH溶液. |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com