
ĚâÄżÁбí(°üŔ¨´đ°¸şÍ˝âÎö)
27ˇ˘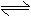 ¸ßÂŻÁ¶ĚúÖĐ·˘ÉúµÄ»ů±ľ·´Ó¦ČçĎÂŁşFeO(s)+CO(g)ˇˇˇˇˇˇ Fe(s)+CO2(g)¨DQˇŁĆäĆ˝şâłŁĘýżÉ±í´ďÎŞŁşK=c(CO2)/c(CO)Ł¬ŇŃÖŞ1100ˇćŁ¬K=0.263
¸ßÂŻÁ¶ĚúÖĐ·˘ÉúµÄ»ů±ľ·´Ó¦ČçĎÂŁşFeO(s)+CO(g)ˇˇˇˇˇˇ Fe(s)+CO2(g)¨DQˇŁĆäĆ˝şâłŁĘýżÉ±í´ďÎŞŁşK=c(CO2)/c(CO)Ł¬ŇŃÖŞ1100ˇćŁ¬K=0.263
(1)ζČÉý¸ßŁ¬»ŻŃ§Ć˝şâŇƶŻşó´ďµ˝ĐµÄĆ˝şâŁ¬¸ßÂŻÄÚCO2şÍCOµÄĚĺ»ý±ČÖµ________Ł¬Ć˝şâłŁĘýKÖµ________(±ľĐˇĚâżŐ¸ńĚÔö´óˇ±ˇ°ĽőСˇ±»ňˇ°˛»±äˇ±)
(2)1100ˇćʱŁ¬˛âµĂ¸ßÂŻÖĐc(CO2)=0.025mol/LŁ¬c(CO)=0.1mol/LŁ¬ÔÚŐâÖÖÇéżöϸ÷´Ó¦ĘÇ·ń´¦ÓÚĆ˝şâ״̬_________(ĚĘǡ±»ňˇ°·ńˇ±)Ł¬´Ëʱ»ŻŃ§·´Ó¦ËŮÂĘĘÇVŐý ______VÄć(Ě´óÓÚˇ±ˇ˘ˇ°ĐˇÓÚˇ±»ňˇ°µČÓÚˇ±)Ł¬ĆäÔŇňĘÇ_________________ˇŁ
26ˇ˘Ľ×ˇ˘ŇŇĘǶţÖÖłŁĽűµÄ¶ĚÖÜĆÚÔŞËصĵĄÖĘŁ¬ËüĂǵÄĐÔÖĘČçĎÂÍĽˇŁĆäÖĐCÎŞ°×É«łÁµíŁ¬DÎŞĆřĚ塣
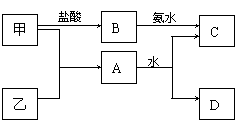 (1)ČôDÎŞËáĐÔĆřĚ壬ÔňAµÄ»ŻŃ§Ę˝ÎŞ___ˇŁ
(1)ČôDÎŞËáĐÔĆřĚ壬ÔňAµÄ»ŻŃ§Ę˝ÎŞ___ˇŁ
(2)ČôDÎŞĽîĐÔĆřĚ壬ÔňA+H2OˇúC+DµÄ»ŻŃ§·˝łĚʽΪ_____________ˇŁ´ËʱÉúłÉ1molĆřĚĺDŁ¬Í¬Ę±µĂµ˝____molłÁµíCˇŁ
(3)ČôÓÉ2ÖÖÔŞËŘ×éłÉµÄ»ŻşĎÎďM·˘ÉúË®˝âŁ¬Ö»ÉúłÉ2ÖÖËáXşÍYŁ¬ĎÂĎÂÁĐ˵·¨ÖĐŐýČ·µÄĘÇ____________(ĚîĐňşĹ)ˇŁ
˘ŮMżÉÄÜÓÉÁ˝ÖÖ·Ç˝đĘô×éłÉ
˘ÚXˇ˘YŇ»¶¨ÎŞŇ»ÔŞËᡡˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇ ˘ŰMŇ»¶¨ş¬ÓĐ˝đĘôÔŞËŘ
˘Ü´Ë·´Ó¦żÉÄÜÎŞŃő»Ż»ąÔ·´Ó¦ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˘ÝÉúłÉÎďÖĐÎŢŃőËᣬş¬ŃőËᲢ´ćˇŁ
25ˇ˘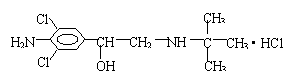 ˇ¶»ŻŃ§˝ĚÓýˇ·µÚĘ®ĆÚ±¨µŔÁËĘýĆđŇňĘłÓĂÓС°ĘÝČâľ«ˇ±µÄÖíČâşÍÄÚÔ࣬¶ř·˘ÉúĽ±ĐÔÖжľµÄ¶ńĐÔĘÂĽţˇŁŐâ×ăŇÔ˵Ă÷Ł¬ÄżÇ°ÓÉÓÚĽéÉ̵ÄÎĄ·¨ľÓŞŁ¬ŇŃĘąˇ°ĘÝČâľ«ˇ±±äłÉÁˡ°ş¦ČËľ«ˇ±ˇŁˇ°ĘÝČâľ«ˇ±µÄ˝áąążÉ±íʾΪŁş
ˇ¶»ŻŃ§˝ĚÓýˇ·µÚĘ®ĆÚ±¨µŔÁËĘýĆđŇňĘłÓĂÓС°ĘÝČâľ«ˇ±µÄÖíČâşÍÄÚÔ࣬¶ř·˘ÉúĽ±ĐÔÖжľµÄ¶ńĐÔĘÂĽţˇŁŐâ×ăŇÔ˵Ă÷Ł¬ÄżÇ°ÓÉÓÚĽéÉ̵ÄÎĄ·¨ľÓŞŁ¬ŇŃĘąˇ°ĘÝČâľ«ˇ±±äłÉÁˡ°ş¦ČËľ«ˇ±ˇŁˇ°ĘÝČâľ«ˇ±µÄ˝áąążÉ±íʾΪŁş
(1)Ćä·Ö×ÓʽΪ_____________________ˇŁ
(2)Ëü˛»żÉÄÜ·˘ÉúµÄ·´Ó¦ÎŞ___________ˇŁ
AŁ®Ë®˝â·´Ó¦ˇˇ BŁ®ĽÓłÉ·´Ó¦ˇˇ CŁ®ÓëÄĆ·´Ó¦·ĹłöÇâĆřˇˇ DŁ®ĽÓľŰ·´Ó¦
(3)´Ó˝áąąÉĎ·ÖÎöŁ¬¸ĂÎďÖʿɿ´×÷_________ŔŕÎďÖʡŁ
AŁ®·ĽĎă×廯şĎÎˇˇˇˇ BŁ®´Ľˇˇˇˇˇˇ CŁ®Â±´úĚţˇˇˇˇˇˇ DŁ®°±»ůËá
˘Ůˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
˘Úˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
˘Űˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
24ˇ˘(20·Ö)ŇÔĎÂĘÇŃĐľżĐÔѧϰµÄ2¸öżÎĚ⣺
(1)żĆѧŃĐľż·˘ĎÖŁ¬ČËĂÇł¤ĆÚ˝Ó´ĄŐâÖÖłý˛ÝĽÁ»ĽÄłÖÖ°©Ö˘µÄżÉÄÜĐÔŇŞÔ¶Ô¶¸ßÓÚδ˝Ó´ĄŐߡŁĂŔąúżĆѧĽŇ´ÓŇ»ÖÖϸľúµÄDNAÖĐ·ÖŔëµĂµ˝ÁËÄÜ˝µ˝â2,4ŁDłý˛ÝĽÁµÄ»ůŇňƬ¶ÎŁ¬˝«ĆäתŇƵ˝ÁíŇ»ÖÖϸľúϸ°űÄÚŁ¬»ńµĂÁËÄܸßЧ˝µ˝â2,4ŁDłý˛ÝĽÁµÄת»ůŇňľúˇŁľÝ´Ë»Ř´đŁş
˘Ů2,4ŁDĽČÄÜ´Ů˝řË«×ÓҶֲÎďÉúł¤ÓÖÄÜɱËŔË«×ÓҶֲÎďµÄÔŇňĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
˘Ú¸Ăת»ůŇňľúÄܱíĎÖҲ˝µ˝â2,4ŁDµÄĐÔ×´˛˘ÄÜ´ú´úĎŕ´«Ł¬Ëů×ńѵÄÉúÎďѧÔŔíĘǡˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
˘ŰČËĂÇÔÚÉú˛úÉϲ»Ö±˝ÓÓ¦ÓĂ×îÔç·˘ĎֵľßÓĐ˝µ˝â»ůŇňµÄϸľúŁ¬¶řĘÇĹŕÓýşÍÓ¦ÓĂת»ůŇňľúŔ´˝µ˝âłý˛ÝĽÁµÄżÉÄÜÔŇňĘÇŁ¬×Ş»ůŇňľúÓëÔϸľúĎŕ±ČÓĐČçĎÂĚص㣺ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
(2)×ĘÁĎĎÔĘľŁ¬˝ü10ÄęŔ´Ł¬PCRĽĽĘő(ľŰşĎøÁ´·´Ó¦)łÉÎŞ·Ö×ÓÉúÎďѧʵŃéĘҵÄŇ»ÖÖłŁąćʵŃéĘֶΣ¬ĆäÔŔíĘÇŔűÓĂDNA°ë±ŁÁô¸´ÖƵÄĚŘĐÔŁ¬ÔÚĘÔąÜÖĐ˝řĐĐDNAµÄČËą¤¸´ÖĆ(ČçĎÂÍĽ)Ł¬Ôں̵ܶÄʱĽäÄÚŁ¬˝«DNAŔ©ÔöĽ¸°ŮÍň±¶ÉőÖÁĽ¸Ę®ŇÚ±¶Ł¬ĘąĘµŃéĘŇËůĐčµÄŇĹ´«ÎďÖʲ»ÔŮĘÜĎŢÓÚ»îµÄÉúÎďĚ塣ÇëľÝÍĽ»Ř´đŁş
˘ŮĽÓČČÖÁ94ˇćµÄÄżµÄĘÇĘąDNAÖеÄ___Ľü¶ĎÁŃŁ¬ŐâŇ»ąýłĚÔÚϸ°űÄÚĘÇͨąý_____µÄ×÷ÓĂŔ´ÍęłÉµÄˇŁ
˘Ú×ŰşĎPCRĽĽĘőÓëČËĚĺϸ°űÄÚDNAşĎłÉąýłĚżÉÖŞŁ¬¶ţŐߵıŘĐčĚőĽţÖĐŁ¬łýÁËÄŁ°ĺˇ˘ÔÁϡ˘ATPˇ˘Ă¸ŇÔÍ⣬ÖÁÉŮ»ąÓĐ3¸öĘÇ______________________________ˇŁ
˘ŰPCRĽĽĘő˛»˝öÎŞŇĹ´«˛ˇµÄŐď¶Ď´řŔ´Á˱ăŔűŁ¬¶řÇҸĽřÁËĽě˛âϸľúşÍ˛ˇ¶ľµÄ·˝·¨ˇŁČôŇŞĽě˛âŇ»¸öČËĘÇ·ń¸ĐČľÁË°¬×̲ˇ¶ľŁ¬ÄăČĎÎŞżÉÓĂPCRĽĽĘőŔ©ÔöËűŃŞŇşÖеÄ
AŁ®°×ϸ°űDNAˇˇˇˇ BŁ®˛ˇ¶ľµÄµ°°×Öʡˇˇˇˇˇˇˇ CŁ®ŃŞ˝¬ÖеĿąĚ塡ˇˇˇˇ DŁ®˛ˇ¶ľµÄşËËá
˘Ůˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
˘Úˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇ ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
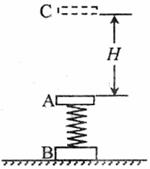
34Ł®(19·Ö)Aˇ˘BÁ˝¸öľŘĐÎÄľżéÓĂÇᵯ»ÉĎŕÁ¬˝ÓŁ¬µŻ»ÉµÄľ˘¶ČϵĘýÎŞkŁ¬ÄľżéAµÄÖĘÁżÎŞmŁ¬ÄľżéBµÄÖĘÁżÎŞ2mˇŁ˝«ËüĂÇĘúÖ±µţ·ĹÔÚˮƽµŘĂćÉĎŁ¬ČçÍĽËůĘľˇŁ
ˇˇ (1)ÓĂÁ¦˝«ÄľżéA»şÂýµŘĘúÖ±ĎňÉĎĚáĆđŁ¬ÄľżéAĎňÉĎĚáĆđ¶ŕ´ó¸ß¶ČʱŁ¬ÄľżéB˝«Ŕ뿪ˮƽµŘĂ档
ˇˇ (2)Čçąű˝«ÁíŇ»żéÖĘÁżÎŞmµÄÎďżéC´ÓľŕÄľżéA¸ßH´¦×ÔÓÉÂäĎÂŁ¬CÓëAĎŕĹöşóŁ¬Á˘Ľ´ÓëAŐłÔÚŇ»Ć𣬲»ÔŮ·ÖżŞŁ¬ÔŮ˝«µŻ»ÉŃąËőŁ¬´ËşóŁ¬Aˇ˘CĎňÉϵŻĆđŁ¬×îÖŐÄÜʹľżéB¸ŐşĂŔ뿪µŘĂ档ČçąűÄľżéCµÄÖĘÁżĽőÎŞm/2Ł¬ŇŞĘąÄľżéB˛»Ŕ뿪ˮƽµŘĂ棬ÄÇ
 ˇˇ
Ă´ÄľżéC×ÔÓÉÂäϵĸ߶ČhľŕA˛»ÄÜł¬ąý¶ŕÉŮŁż
ˇˇ
Ă´ÄľżéC×ÔÓÉÂäϵĸ߶ČhľŕA˛»ÄÜł¬ąý¶ŕÉŮŁż
33.(20·Ö)˘ń.(14·Ö)şěČȵÄĚúÄÜÓëË®ŐôĆř·´Ó¦Ł¬ÓĐÇâĆřÉúłÉŁ¬ĎÖÓĂĎÂÍĽËůĘľ×°ÖĂ˝řĐĐĚúÔÚ¸ßÎÂĎÂÓëË®ŐôĆř·´Ó¦µÄʵŃ飬˛˘ÓĂĽňµĄµÄ·˝·¨ĘŐĽŻŁ¬ĽěŃéÉúłÉµÄÇâĆřˇŁÇë»Ř´đĎÂÁĐÎĘĚ⣺ˇˇ
(1)(3·Ö)Đ´łöĚúÔÚ¸ßÎÂĎÂÓëË®ŐôĆř·´Ó¦µÄ»ŻŃ§·˝łĚĘ˝ ˇˇˇˇˇˇˇˇˇˇˇˇˇŁˇˇ
(2)(3·Ö)¸ÉÔďąÜCÄÚʢ·ĹµÄŇ©Ć·ĘÇ ˇˇˇˇˇˇˇˇˇˇˇˇ»ň ˇˇˇˇˇˇˇˇˇˇˇˇ(Ěѧʽ)ˇŁ¸ÉÔďąÜµÄˇˇˇˇˇˇˇˇˇˇ ˇˇ(m»ňn)¶ËÓëgµĽąÜĎŕÁ¬˝ÓˇŁˇˇ
(3)(4·Ö)ÔÚD´¦»łöÓĂĽňµĄ·˝·¨ÓĂĘÔąÜŔ´ĘŐĽŻÇâĆřµÄ×°ÖĂÍĽ(ËůĐčĆäËűŇÇĆ÷×ÔĽşŃˇÔń)ˇˇ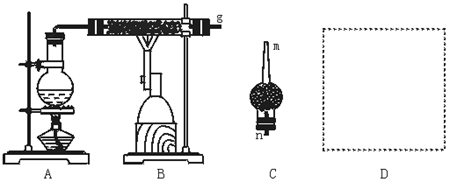
ˇˇ(4)(4·Ö)ÔőŃůÓĂĽňµĄ·˝·¨ĽěŃéĘŐĽŻµ˝µÄĆřĚĺĘÇÇâĆřŁ¬ĽňĘöʵŃé˛Ů×÷˛˝ÖčşÍĎÖĎ󡡡ˇˇˇˇˇˇˇˇˇ ˇŁˇˇ
˘ň.(6·Ö)ÉčĽĆĽňµĄĘµŃé˵Ă÷ĎÂÁĐÎďÖʵÄŃő»ŻĐÔÓÉÇżµ˝ČőµÄËłĐňÎŞŁşCl2ŁľFeCl3ŁľKIżÉѡÓõÄŇ©Ć·ÓĐŁşÂČË®ˇ˘FeCl3ČÜŇşˇ˘µâË®ˇ˘KIČÜŇşˇ˘NaOHČÜŇşˇ˘ĎˇÁňËᡢŃÎËᡢKSCNČÜŇşˇ˘µâ»ŻĽŘµí·ŰČÜŇşˇ˘FeCl2ČÜŇşˇ˘H2O2ˇ˘Ë®µČˇŁËůĐčŇÇĆ÷×ÔÓÉѡÔńˇŁĽňĘöʵŃ鲽Ö衢ĎÖĎ󡢽áÂŰŁ»ˇˇ
(1)(3·Ö) ˇˇˇˇˇˇˇˇˇˇˇˇˇŁˇˇ
(2)(3·Ö) ˇˇˇˇˇˇˇˇˇˇˇˇˇŁ
32.(13·Ö)Äłł§·ĎŇşÖĐş¬ÓĐ´óÁżAg+ˇ˘Fe3+ˇ˘Al3+Ł¬ÓĂĎÂÍĽ·˝·¨˝řĐĐ·ÖŔë(˛ż·Ö·´Ó¦Ěő
 ĽţʡÂÔ)Łş
ĽţʡÂÔ)Łş
ˇˇ (1)Đ´łöĎÂÁĐÎďÖʵĻŻŃ§Ę˝Łş
ˇˇˇˇˇˇˇˇ ĘÔĽÁxˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇ˘ĘÔĽÁzˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
ˇˇˇˇˇˇˇˇ ľ§ĚĺEˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇ˘ąĚĚĺGˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁ
ˇˇ (2)Đ´łöĎÂÁĐ·´Ó¦µÄŔë×Ó·˝łĚĘ˝Łş
ˇˇˇˇˇˇˇˇ łÁµíA+ĘÔĽÁyŁşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
ˇˇˇˇˇˇˇˇ ÂËŇşD+ąýÁżCO2Łşˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
31.(11·Ö)ijúÖĐş¬ÓĐÁňÔŞËŘŁ¬ĂşÔÚČĽÉŐąýłĚÖĐÄܲúÉú»áŇýĆđËáÓęµÄĆřĚĺAˇŁÎŞ˝µµÍĆřĚĺAµÄĹĹ·ĹÁżŁ¬˛ÉȡµÄ´ëʩ֮һľÍĘÇĎňĂşÖĐĽÓÉúĘŻ»ŇŁ¬´Ë·¨łĆÎŞˇ°¸Ć»ůąĚÁňˇ±ˇŁŐâÖÖúȼÉպ󣬴󲿷ÖÁňÔŞËŘ×îÖŐŇÔCaSO4µÄĐÎĘ˝´ćÔÚˇŁˇˇ
(1)(3·Ö)ČôĂşÖĐş¬ÁňÁżÎŞ0.32%(ÖĘÁż·ÖĘý)Ł¬´¦Ŕí1 tŐâÖÖĂşŁ¬Ó¦ÖÁÉŮĽÓČë´ż¶ČÎŞ96%µÄÉúĘŻ»Ňˇˇˇˇ ˇˇˇˇˇˇˇˇkgˇŁˇˇ
(2)(4·Ö)ÔÚżŐĆřÎŰČľĽŕ˛âÖĐŁ¬łŁÓĂBr2ÓëĆřĚĺAµÄ¶¨Áż·´Ó¦Ŕ´˛â¶¨żŐĆřÖĐAµÄş¬ÁżˇŁĐ´łöË®ČÜŇşÖĐBr2ÓëĆřĚĺA·´Ó¦µÄ»ŻŃ§·˝łĚĘ˝Łşˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁˇˇ
(3)(4·Ö)ÉĎĘö·´Ó¦ÖеÄBr2ĘÇÓÉŇ»¸ö×°ÓĐËáĐÔä廯ĽŘČÜŇşµÄµç˝â˛ŰĚáą©ˇŁµ±˝«ÄłÖÖżŐĆřŇÔ1.2ˇÁ10-4 m3/minµÄÁ÷ËŮͨČëµç˝â˛ŰµÄŃôĽ«ĘŇŁ¬µçÁ÷ĽĆĎÔʾΪ7.5ˇÁ10-6 AʱŁ¬´ËĽ«ĘŇÖĐBr2µÄŨ¶Č±ŁłÖ˛»±äˇŁ´ËÖÖżŐĆřÖĐSO2µÄş¬ÁżĘÇ ˇˇˇˇˇˇˇˇˇˇˇˇmgˇ¤m-3ˇŁˇˇ
30. (12·Ö)ŇŃÖŞ(CH3)2C===CHCH2CH3ˇˇˇˇˇˇˇˇˇˇ
ˇˇCH3COCH3+CH3CH2COOH
(12·Ö)ŇŃÖŞ(CH3)2C===CHCH2CH3ˇˇˇˇˇˇˇˇˇˇ
ˇˇCH3COCH3+CH3CH2COOH
CH2==CHCH==CH2 + CH2==CH2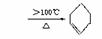
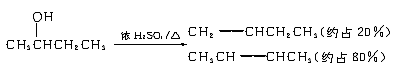
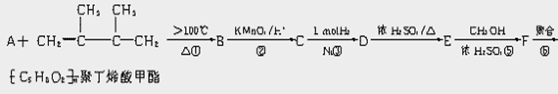 Ň»ÖÖŔŕËĆÓĐ»ú˛ŁÁ§µÄËÜÁĎ--ľŰ¶ˇĎ©ËáĽ×őĄÓĐąă·şÓĂÍľˇŁşĎłÉËüÓв»Í¬µÄÍľľ¶Ł¬ŇÔĎºϳɵĸ±˛úĆ·´ó¶ŕÎŞµÍĽ¶ÎŰČľÎď»ňÎŢÎŰČľÎÔ×ÓŔűÓĂÂʽϸߣ¬·űşĎˇ°ÂĚÉ«»ŻŃ§ˇ±µÄŇŞÇóˇˇ
Ň»ÖÖŔŕËĆÓĐ»ú˛ŁÁ§µÄËÜÁĎ--ľŰ¶ˇĎ©ËáĽ×őĄÓĐąă·şÓĂÍľˇŁşĎłÉËüÓв»Í¬µÄÍľľ¶Ł¬ŇÔĎºϳɵĸ±˛úĆ·´ó¶ŕÎŞµÍĽ¶ÎŰČľÎď»ňÎŢÎŰČľÎÔ×ÓŔűÓĂÂʽϸߣ¬·űşĎˇ°ÂĚÉ«»ŻŃ§ˇ±µÄŇŞÇóˇˇ
(1)(8·Ö)Đ´łö˝áąąĽňĘ˝ŁşAˇˇˇˇˇˇˇˇˇˇˇˇ B ˇˇˇˇˇˇˇˇˇˇˇˇˇˇC ˇˇˇˇˇˇˇˇˇˇˇˇ
D ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ
(2)(2·Ö)Đ´łöEˇúFµÄ»ŻŃ§·´Ó¦·˝łĚĘ˝ ˇˇˇˇˇˇˇˇˇˇˇˇˇŁˇˇ
(
3)(2·Ö)ÔÚˇ°ÂĚÉ«»ŻŃ§ˇ±ÖĐŁ¬ŔíĎë״̬ĘÇ·´Ó¦ÎďÖĐÔ×ÓČ«˛ż×Ş»ŻÎŞÓűÖƵõIJúÎĽ´Ô×ÓŔűÓĂÂĘÎŞ100%Ł¬ŔýČ磺ĽÓłÉ·´Ó¦µČˇŁÉĎĘöşĎłÉąýłĚŁ¬·űşĎˇ°ÂĚÉ«»ŻŃ§ˇ±ŇŞÇóµÄ·´Ó¦ÓĐ(ĚîĐ´·´Ó¦ĐňşĹ)ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇŁˇˇ
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com