
【题目】在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如下表所示:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量/g | 12 | 26 | 3 | 0 |
反应中的质量/g | 9 | 22 | 3 | b |
反应后的质量/g | 0 | a | 3 | 28 |
下列说法正确的是( )
A.a等于10 B.该化学反应为复分解反应 C.丙一定为催化剂 D.b等于12
科目:初中化学 来源: 题型:
【题目】如图是a.b、c三种物质的溶解度曲线,下列有关说法不正确的是( )

A.P点表示t1℃时a和c的溶解度均为20g
B.t2℃时,溶质质量分数为30%的a溶液是饱和溶液
C.从a和c的混和溶液中提纯a,可采用降温结晶的方法
D.将t1℃时a、b、c的饱和溶液分别升温到t2℃,所得溶液中溶质的质量分数大小顺序为:b>a>c
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图中甲~戊是初中化学教材中常见物质。甲、戊为氧化物且甲为黑色固体,乙、丙分别是酸和碱中的一种,丁是大理石的主要成分。(图“—”表示相连的物质间可发生反应,“→”表示一种物质可转化为另一种物质,反应条件、部分反应物与生成物均已略去。)下列说法中不正确的是

A.乙溶液能使紫色石蕊溶液变红 B.丙溶液能与戊反应生成丁
C.甲→戊只能通过置换反应实现 D.不能由甲通过一步反应生成丁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是_________。
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为________,水的体积为________mL (水的密度近似看作1g/cm3)。
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如右下图.t1℃时,甲物质的溶解度是________。t2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是________(填“甲”或“乙”)物质的饱和溶液。

选项 | x | y |
A | 水 | 氧化钙 |
B | 水 | 硝酸铵 |
C | 浓硫酸 | 水 |
D | 稀盐酸 | 镁 |
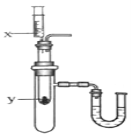
(4)按右上图所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】苏州盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为Cl9Hl9N7O6。下列有关叶酸的说法中正确的是
A.叶酸的相对分子质量为441 g
B.叶酸中氮元素的质量分数大于氧元素的质量分数
C.叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6
D.叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“细菌冶金”的原理是利用氧化铁硫杆菌促使 黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并能为CO2和H2O合成有机物提供能量.流程如图,下列说法错误的是( )

A.反应①化学方程式:4FeS2+15O2+2X=2Fe2(SO4)3+2H2SO4,X为H2O2
B.整个流程提高了能量的利用率
C.图中有机物一定不含氧元素
D.氧化铁硫杆菌在反应①中起催化作用
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.
研究主题:水溶液中复分解反应的实质
相关信息:一定体积的溶液中,离子的数目越多,其离子的浓度越大.电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小.相同温度下同种溶液电导率越大,离子浓度越大.
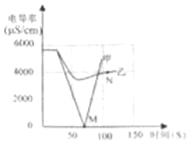
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示.
①写出Ba(OH)2与H2SO4反应的化学方程式 .
②甲曲线M点时混合液体呈 色;
③通过对甲曲线的分析,下列说法错误的是 (填序号).
A.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4
B.M点时离子浓度几乎为零 C.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示.
①通过对乙曲线的分析,下列说法错误的是 (填序号).
A.开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B.电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
C.整个实验过程中,溶液中Na+数目一直增大
②N点时,溶液中含有的离子是 (填离子符号).
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度 (填“增大”或“减小”).
(3)拓展:①请根据示例仿写离子方程式.
示例AgNO3+NaCl=AgCl↓+NaNO3离子方程式:Ag++Cl﹣=AgCl↓
仿写:BaCl2+Na2SO4=BaSO4↓+2NaCl离子方程式: .
②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊后浑浊逐渐消失.请推测此过程的溶液中Ca2+的浓度变化情况 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图为甲、乙两种固体物质(不考虑结晶水) 的溶解度曲线。下列说法错误的是
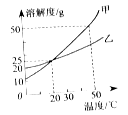
A.20 ℃时,甲、乙具有相同的溶解度
B.甲、乙的溶解度都随温度的升高而增大
C.20 ℃时,可以配制溶质的质量分数为25%的甲溶液
D.50℃时,甲和乙各30g分别加入100g水中,充分溶解后同时等速降温,则乙溶液中先有固体出现
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按下列方法配制的溶液,其溶质质量分数为5%的是
A.称取5.0g氯化钾,溶解在95mL水中,充分搅拌
B.称取5.0g生石灰,放入95mL水中,充分搅拌
C.量取5.OmL浓盐酸,倒入95mL水中,充分搅拌
D.称取5.0g二氧化锰,放入95mL水中,充分搅拌
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com