
【题目】下列图像表述的化学事实与实际相符的是
A | B | C | D | |
图象 |
|
|
|
|
实验或事实 | 向pH=12的Ca(OH)2溶液中不断加水稀释 | 20C时,向一杯不饱和的KNO3溶液中逐步加入KNO3晶体 | 向稀盐酸中滴加过量的烧碱溶液 | 将一定质量的MnO2和KClO混合加热 |
A. AB. BC. CD. D
【答案】D
【解析】
A、向pH=12的Ca(OH)2溶液中不断加水稀释,pH会减小,但是不会小于等于7,图像与事实不符,故A错误;
B、20℃时,向一杯不饱和的KNO3溶液中逐步加入KNO3晶体,开始时,溶质的质量分数不为零,硝酸钾继续溶解,直至饱和,溶质质量分数是逐渐增大到不变,图像与事实不符,故B错误;
C、向稀盐酸中滴加过量的烧碱溶液,开始时的pH应该是小于7,图像与事实不符,故C错误;
D、将一定质量的MnO2和KClO混合加热,开始MnO2质量分数不为零,氯酸钾在二氧化锰的催化作用下受热生成氯化钾和氧气,二氧化锰质量在反应前后不变,剩余固体的质量不断减小,MnO2质量分数不断增大,反应结束后不变,图像与事实相符,故D正确。故选D。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】2018年12月24日,世界最大水陆两栖飞机AG600从珠海一飞冲天,中国大飞机“三兄弟”终于蓝天聚首。AG600建造中采用了大量的钛合金。
(1)钛和钛合金被认为是21世纪的重要金属材料,具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,钛合金与人体有很好的“相容性”,但价格昂贵。根据它们的主要性能,下列用途不切合实际的是_________(填序号)。
A作电路保险丝 B制造航天飞机 C制作假肢 D制造船舶
(2)为研究Cu、Ti、Fe三种金属的活动性顺序,甲、乙两同学设计了如下方案(金属片已打磨)。
①方案一:甲同学将三种大小相同的金属片分别加入盛有等体积等浓度稀硫酸的3支试管中,根据铜加入稀硫酸中无明显现象以及_____________________________的现象,判断出Ti>Fe>Cu。已知钛元素在化合物中常显+4价,写出钛和稀硫酸反应的化学方程式:____________________________。
②方案二:乙同学只用一支试管,只取一次硫酸,也能证明Ti>Fe>Cu,他插入金属的顺序是:Fe、_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学用如图所示装置.分别进行“燃烧条件”和“氧气性质”的探究实验(已知:白磷的着火点为40℃)。请回答下列问题:
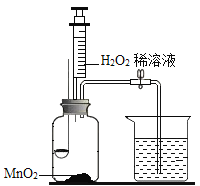
内容步骤 | (实验1)燃烧条件 | (实验2)氧气性质 |
1 | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞; | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞; |
2 | 推入H2O2溶液 | 推入H2O2溶液 |
(1)H2O2与MnO2接触时,发生反应的化学方程式为___________________,MnO2起_________作用。
(2)实验1中,推入H2O2溶液,燃烧匙和水中的白磷均不燃烧,原因分别是___、____;打开止水夹,推入H2O2溶液,观察到烧杯中的现象是_______。
(3)实验2中打开止水夹,推入H2O2溶液,观察到木炭燃烧得更剧烈,由此得出氧气的性质是_______,木炭熄灭冷却一段时间后,烧杯中的部分溶液流入集气瓶,该实验开始时到实验结束后,集气瓶内压强的变化过程是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组为验证“氨气还原氧化铜”的实验,认真查阅资料并做出以下准备。
资料准备:
I.氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,溶液呈碱性。
Ⅱ.氨气在加热的条件下还原氧化铜,有三种生成物:一是金属单质,二是空气中含量最多的气体,三是相对分子质量最小的氧化物。
实验准备:
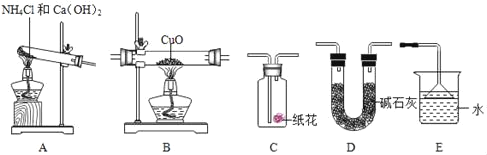
请回答:
(1)为达成“氨气还原氧化铜”的实验目的,装置A、B、D、E的正确连接顺序_____(填序号)。
(2)装置A中发生反应的化学方程式_____。
(3)装置B观察到的现象_____,其反应的化学方程式为_____;装置E的作用_____。
(4)若将装置A产生的气体通入装置C中,石蕊试液浸泡的纸花变_____色。
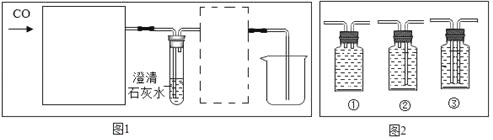
(5)若实验室用一氧化碳还原氧化铜,应选上述装置_____(填序号)与下列图1中的_____装置连接,则该装置玻璃管内发生反应的化学方程式是_____,实验时要先通CO再加热的目的是防止一氧化碳和空气混合加热时发生爆炸。图1虚线框内的装置是用于吸收CO2,并收集CO,应选择图2(广口瓶内均为氢氧化钠溶液)中的装置_____(填序号)最合适。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】白钨矿的主要成分是CaWO4,工业上用白钨矿生产钨的流程如图所示:
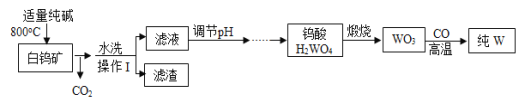
(查阅资料)
CaWO4与纯碱发生反应的化学方程式是CaWO4+Na2CO3═Na2WO4+CaO+CO2↑。
(1)反应前需要将白钨矿进行粉碎,其目的是_____;
(2)水洗后进行的分离操作中,所用的玻璃仪器有烧杯、_____和玻璃棒,其中玻璃棒的作用是_____;
(3)上述滤液的成分中含有氢氧化钙,写出生成该物质的反应的化学方程式:_____;
(4)三氧化钨与氢气反应时,表现出还原性的物质是_____写出金属钨的一种用途:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图像分别对应四个变化,其中正确的是
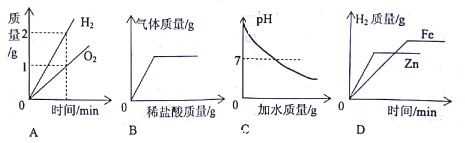
A. 将水通电一段时间后
B. 向氢氧化钾和碳酸钾的混合溶液中滴加过量稀盐酸
C. 向一定质量分数的氢氧化钠溶液中不断加水
D. 分别向等质量的铁粉和锌粉中加入过量的相同质量分数的稀硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】ZnSO4饱和溶液的溶质质量分数随温度变化的曲线如图所示.下列说法正确的是( )
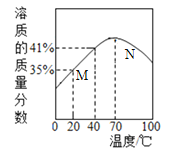
A. N 点对应的 ZnSO4 溶液升温或降温均都可能析出晶体
B. M 点对应的 ZnSO4 溶液是不饱和溶液
C. ZnSO4 饱和溶液的溶质质量分数随温度升高而增大
D. 40℃时,ZnSO4 的溶解度为41g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】见图,在已调平的托盘天平两边各放一个等质量的烧杯,向烧杯中各加入一定量的等质量、等浓度的稀硫酸,然后在左盘的烧杯A中放入一定质量的Zn片,同时在右盘的烧杯B中放入与Zn片等质量的Fe片。

(1)反应后烧杯B中的溶液变____色。
(2)若锌和93.7g稀硫酸恰好完全反应生成0.2g氢气,则反应后所得溶液的溶质质量分数为_____?(请写出运算过程)
(3)在上述实验中,研判托盘天平指针的最终偏向和药品的剩余情况可用下面的方式 来讨论进行:把反应物的质量处理成粒子数,再通过讨论硫酸分子的数目范围,最 终确定哪种反应情况,具体见下图:

①上图中甲物质是___(填“Zn”或“Fe”)
②当硫酸分子个数为a时,反应结束后,天平指针最终指在分度盘的______填“左边”或“右边”或“正中央”),A、B两杯中反应剩余物质分别是___;
③当硫酸分子个数≥d 时,请描述在整个实验过程中指针的变化情况:____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com