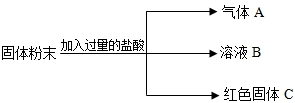
有一包固体粉末,可能由KCl、BaCl2、CuSO4、Na2SO4、Na2CO3中的一种或几种组成.
已知:
(1)若将固体粉末加到水中,得到无色溶液和白色沉淀:由此可知该粉末一定没有______;
(2)过滤,将白色沉淀与稀硝酸混合,沉淀部分溶解.由此可知该粉末一定有______;写出沉淀溶解的化学方程式:______.
【答案】分析:根据各物质之间的反应现象和反应规律分析:硫酸铜溶液呈蓝色,碳酸钡溶于稀硝酸,硫酸钡不溶于稀硝酸.
解答:解:取少量粉末,加水溶解得无色溶液,说明没有硫酸铜.得到白色沉淀,白色沉淀部分溶于硝酸并有气体生成,说明沉淀是碳酸钡沉淀和硫酸钡沉淀的混合物,白色固体中肯定含有氯化钡、硫酸钠和碳酸钠,氯化钾存在与否对实验现象没有影响,故可能含有氯化钾.
(1)若将固体粉末加到水中,得到无色溶液和白色沉淀:由此可知该粉末一定没有CuSO4;
(2)过滤,将白色沉淀与稀硝酸混合,沉淀部分溶解.由此可知该粉末一定有氯化钡、硫酸钠和碳酸钠,碳酸钡溶于稀硝酸生成硝酸钡、水和二氧化碳,化学方程式BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑;
故答案为:(1)CuSO4;(2)BaCl2、Na2SO4、Na2CO3;BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑;
点评:解答本题要从物质的颜色、物质之间相互作用时的实验现象等方面进行分析、判断,从而得出正确的结论.