


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:初中化学 来源: 题型:
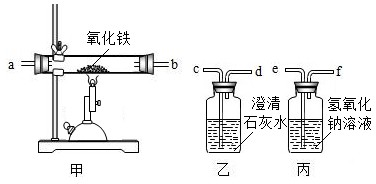
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
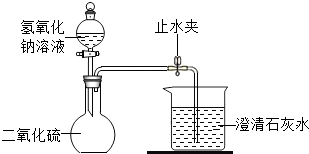 某化学兴趣小组的同学决定探究二氧化硫、亚硫酸钠(Na2SO3)等物质的某些性质.
某化学兴趣小组的同学决定探究二氧化硫、亚硫酸钠(Na2SO3)等物质的某些性质.| 实验操作 | 预期现象及结论 |
从烧瓶内取少量反应后的澄清溶液(或液体)两份,一份加入少量澄清石灰水,另一份加入碳酸钠溶液 从烧瓶内取少量反应后的澄清溶液(或液体)两份,一份加入少量澄清石灰水,另一份加入碳酸钠溶液 |
若加入澄清石灰水后有沉淀生成,则溶质是氢氧化钠和亚硫酸钠;若加入碳酸钠后有沉淀生成,则溶质是氢氧化钠和氢氧化钙;若加入二者后均无明显现象,则溶质是氢氧化钠 若加入澄清石灰水后有沉淀生成,则溶质是氢氧化钠和亚硫酸钠;若加入碳酸钠后有沉淀生成,则溶质是氢氧化钠和氢氧化钙;若加入二者后均无明显现象,则溶质是氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
查看答案和解析>>
科目:初中化学 来源: 题型:
下列表述正确的是
A.含有大量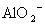 的溶液中:K+、
的溶液中:K+、 、
、 、
、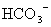 可共存
可共存
B.CO(g)的燃烧热是283.0kJ·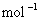 ,则
,则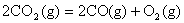 反应的
反应的
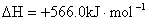
C.将SO2通入 溶液中:
溶液中: +2HClO
+2HClO
D.在某钠盐溶液中含有等物质的量的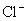 、
、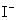 、
、 、
、 、
、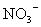 、
、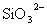 中的一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有
中的一种或多种,当加入过量的盐酸产生气泡,溶液颜色变深但仍澄清,阴离子种数减少3种,则原溶液中一定有
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com