
【题目】如图所示,向小烧杯中通入 CO2,烧杯内 a、c 为湿润的紫色石蕊试纸,b、d 为干燥的紫色石蕊试纸,烧杯外放一只点燃的短蜡烛。
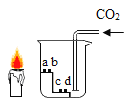
(1)能说明“CO2可与水发生反应”的现象是_______。
(2)下列说法正确的是_______(填字母序号)。
A试纸 c 比 a 先变色,说明 CO2密度大于空气
B一段时间后,蜡烛的火焰逐渐变小至熄灭,可证明 CO2密度大于空气
C若将短蜡烛放在烧杯内,蜡烛熄灭同样可证明 CO2密度大于空气
【答案】a、c的紫色石蕊试纸变红,b、d的紫色石蕊试纸不变红 B
【解析】
(1)二氧化碳能和水反应生成碳酸,碳酸是一种酸,能使紫色石蕊试纸变红。所以向导管通入二氧化碳,湿润的紫色石蕊试纸变色,干燥的紫色石蕊试纸不变色。所以当观察到a、c的紫色石蕊试纸变红,b、d的紫色石蕊试纸不变红,则证明二氧化碳和水反应。故答案为:a、c的紫色石蕊试纸变红,b、d的紫色石蕊试纸不变红;
(2)A、该反应中,二氧化碳通过导管进入烧杯的底部。所以二氧化碳遇到c试纸中的水先反应生成碳酸,使紫色石蕊试纸变红,再经过a使紫色石蕊试纸变红。不能判断出二氧化碳的密度和空气的关系,因为无论气体密度大于空气还是小于空气,气体都会由下而上流动。A错误;
B、一段时间后,烧杯外面的火焰逐渐减小至熄灭,则可以分析出二氧化碳从烧杯中逸出,由于二氧化碳密度大于空气,降到火焰附近。因为二氧化碳不燃烧、不支持燃烧,且密度大于空气,所以蜡烛会熄灭。B正确;
C、若将短蜡烛放在烧杯内,只能证明出二氧化碳不燃烧、不支持燃烧,不能证明出二氧化碳的密度和空气的关系。因为二氧化碳由导管通入,进入了烧杯的底部,无法证明二氧化碳的密度大于空气。C错误。
故答案为:B。


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案科目:初中化学 来源: 题型:
【题目】实验室常利用以下装置完成气体制备及性质实验.请回答:
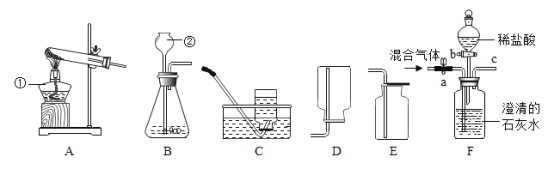
(1)指出编号仪器的名称:①________,②_______.
(2)以上A装置有一处明显的错误,请加以改正_______.利用改正后的装置继续完成后面的实验.
(3)欲使用高锰酸钾制取氧气,应选择的A装置,反应方程式为_____;为防止高锰酸钾粉末进入导管,应采取的措施是__.收集干燥的氧气应选择____。
(4)将CO2和CO的混合气体通过F装置(液体药品均足量),实验开始时关闭活塞b,打开活塞a,广口瓶中观察到的现象石灰水___,此时从导管c逸出的气体主要是一氧化碳.一段时间后,再关闭活塞 a,打开活塞 b,将分液漏斗中的稀盐酸滴入广口瓶中,此时逸出的气体主要是____________,反应方程式为____,欲收集该气体,应选择的装置是____(填字母).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属和金属材料在生产生活中应用广泛。
(1)下列铁制品的用途中,利用金属导热性的是_______(填字母)

(2)目前世界上已有50%以上的废钢铁得到回收利用,其目的是_____________。
A节约金属资源 B合理开采矿物 C防止钢铁生锈
(3)为防止水龙头生锈,其表面镀有一层铬,其做法的原理是_______________。
(4)将生锈的铁制品放入盛有过量稀盐酸的烧杯中,观察到溶液变黄,有无色气泡逸出。写出其中一个反应的化学方程式______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固定物质的溶解度曲线如图所示,下列说法正确的是( )
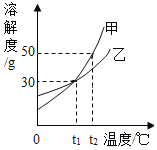
A.在0~t1℃时,甲的溶解度大于乙的溶解度
B.t1℃时,两种物质的溶液中溶质质量分数一定相等
C.t2℃时,150g甲的饱和溶液和100g水混合,所得溶液的溶质质量分数为20%
D.将t2℃时等质量的甲、乙饱和溶液分别降温至t1℃,甲析出固体的质量比乙小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知 KNO3的溶解度如下表所示,下列说法不正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
A.在 10℃-70℃之间,随着温度的升高,KNO3的溶解度增大
B.20℃时,向 100 g 水中加入 35 g KNO3,充分搅拌,所得溶液质量为 131.6 g
C.将 70℃时不饱和的 KNO3溶液降低温度,有可能转化为饱和溶液
D.50℃时,饱和 KNO3溶液中溶质的质量分数为 85.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学小组探究蜡烛在盛有一定体积空气的密闭容器内燃烧时O2和CO含量的变化,测定结果如图所示,下列推理正确的是
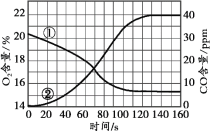
A. 蜡烛由碳、氢元素组成
B. 蜡烛发生了不充分燃烧
C. 曲线①表示CO含量的变化
D. 蜡烛熄灭时,容器内氧气耗尽
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中的①、②分别是镁元素、氯元素在元素周期表中的信息,A、 B、C是三种粒子的结构示意图。试回答下列问题:

(1)镁元素的原子序数是____________,氯元素的相对原子质量是___________________。
(2)A、B、C中化学性质相似的粒子是_____(填序号)。
(3)镁元素和氯元素形成的化合物的化学式是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文
碳元素是最早被人类认识和利用的元素。碳元素在地球上虽然广泛分布,但其含量不足0.03%。碳元素是一切有机体骨架的组成元素,在人体中的含量约占 18%。主要以有机含碳化合物形式存在,如糖类、蛋白质等。人体中的无机含碳化合物种类较少,在血浆中主要以碳酸氢盐缓冲系统 (H2CO3/HCO3-)的形式存在。迄今为止,发现了 15 种碳原子,它们在元素周期表中占据如图 1 所示的同一个“格”,其中 C-12 和C-13 属于稳定型,考古研究中,通过测定 C-14 含量估算古物的年代。20 世纪起,人类对碳元素的认识突飞猛进。下表列出了与之相关的主要事件:碳的这些新型结构的发现和性能研究的发展,使其广泛应用于工业、材料、生物医学等领域。依据文章内容回答下列问题:

时间 | 40 年代 | 1967 年 | 1969 年 | 1985 年 | 1991 年 | 21 世纪 |
事件 | 发现C-14 | 发现六角金刚 石和单斜超硬 碳 | 发现银白色的白炭 | 发现富勒烯 的第一个成 员 C60(图 2) | 发现碳纳米管(图 3) | 从石墨中剥离出仅 由一层碳原子构成 的薄片-石墨烯(图4) |
(1)碳在人体中的存在形式有_______ 种;
(2)关于图 1 所示的相关信息分析,错误的是________;
A 原子序数为 6 B 电子数为 12 C 元素符号为 C
(3)结合你所学的知识,你认为原子 C-12 和 C-13 的不同点是________;
A 质子数不同 B 电子数不同 C 中子数不同
(4)从石墨中剥离出来的石墨烯具有优良的各种性能,被认为是一种未来革命性的材料。石墨和金刚石的物理性质不同的原因是________;
(5)富勒烯 C60 中数字“60”的含义是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com