
| A. | 熔点:青铜、组成青铜的金属铜和锡 | |
| B. | 质子数:铝离子、铝原子 | |
| C. | 生成H2的质量:10g镁与足量盐酸反应、10g铝与足量盐酸反应 | |
| D. | 20℃时:NaOH溶于水后溶液的温度、NH4NO3溶于水后溶液的温度 |
分析 A、根据合金的熔点与其组成成分的熔点比较考虑;
B、根据元素的概念分析;
C、根据化学方程式计算生成氢气的量,然后比较即可;
D、根据NaOH溶于水放热、NH4NO3溶于水吸热分析;
解答 解:A、合金的熔点比它的组成成分熔点要低,故错误;
B、元素是指质子数(核电荷数)相同的一类原子的统称,铝离子和铝原子都属于铝元素,所以其质子数相同,故错误;
C、Mg的相对原子质量为24,24g镁可反应生成2g氢气,即1g镁生成$\frac{1}{12}$克氢气.Al的相对原子质量为27,27g铝可反应生成3g氢气,即1g铝生成$\frac{1}{9}$克氢气.
故10g镁与足量盐酸反应生成H2的质量小于10g铝与足量盐酸反应生成H2的质量.故错误;
D、氢氧化钠溶于水放出热量,温度升高;硝酸铵溶解于水时吸热,温度降低,故正确;
故选:D
点评 本题考查合金的特点,元素的概念,有关化学方程式的计算及物质溶于水后的吸热、放热现象等,要牢固掌握.


科目:初中化学 来源: 题型:填空题
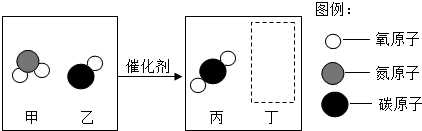
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
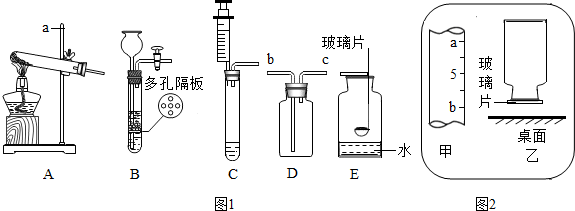
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com