
【题目】向Ba(OH)2溶液中滴入Na2CO3溶液至恰好完全反应。
(1)可以观察到的实验现象是_____
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子。(填离子符号):
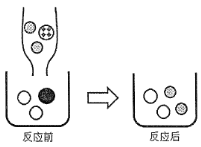
![]() _____
_____![]() _____
_____![]() _____
_____
(3)下列物质中能与Ba(OH)2溶液反应产生沉淀的是_____。(双项选择)
A NaNO3 B HCl C .MgCl2 D (NH4)2SO4
【答案】产生白色沉淀 OH- Ba2+ Na+ CD
【解析】
(1)氢氧化钡溶液与碳酸钠溶液反应生成碳酸钡白色沉淀和氢氧化钠,观察到的实验现象是产生白色沉淀。
(2)向Ba(OH)2溶液中滴入Na2CO3溶液至恰好完全反应,反应的实质是碳酸根离子和钡离子结合生成碳酸钡白色沉淀,则![]() 是Ba(OH)2溶液的钡离子(Ba2+),
是Ba(OH)2溶液的钡离子(Ba2+),![]() 是碳酸钠溶液中的钠离子(Na+),
是碳酸钠溶液中的钠离子(Na+),![]() 是Ba(OH)2溶液中存在的氢氧根离子(OH-)。
是Ba(OH)2溶液中存在的氢氧根离子(OH-)。
(3)Ba(OH)2溶液与NaNO3交换成分没有沉淀、气体或水生成,不能发生复分解反应;
与盐酸发生中和反应生成氯化钡和水;
与MgCl2反应生成氢氧化镁白色沉淀和氯化钡;
与(NH4)2SO4反应生成硫酸钡沉淀和氨气和水。
故答案为:
(1)产生白色沉淀;
(2)OH-;Ba2+;Na+;
(3)CD。


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:初中化学 来源: 题型:
【题目】从2018年3月26日起,我国对原产于美国、欧盟、韩国、日本和泰国的进口苯酚进行反倾销立案调查,苯酚(化学式为C6H6O)常温下通常为无色针状或白色块状晶体,溶于酒精,在室温时稍溶于水腐蚀力强,可燃。苯酚是重要的有机化工原料,主要用于制备酚醛树脂、水杨酸等工业原料,还可以用作溶剂、试剂和消毒剂,广泛运用于合成纤维、塑料、医药、农药、香料、染料、涂料和炼油工业等领域。

根据上述信息,请回答:
①苯酚由_____种元素组成,它属于_____(选填“单质”、“氧化物”、“化合物”、“混合物”中的一项)。
②苯酚中,碳元素和氢元素的质量比为_____(填最简整数比)。
③苯酚中,质量分数最大的元素为_____(填写元素名称)。
④上述有关苯酚性质的描述中,属于化学性质的是_____(写出一项即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】闪锌矿(主要成分为ZnS)经熔烧得锌熔砂,锌熔砂主要含ZnO、ZnFe2O4,以及少量CuO,工业上用其制备金属锌,具体过程如图所示。
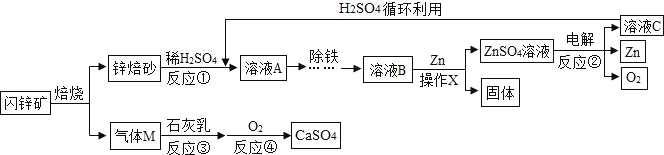
(1)进行反应①时,要将锌熔砂粉粹成细小颗粒,目的是_____。
(2)操作X的名称是_____;经该操作得到的ZnSO4溶液仍然浑浊,可能的原因是_____。
(3)ZnFe2O4可看作两种氧化物的结合物,与稀H2SO4反应产生两种盐,分别是ZnSO4和_____(填化学式)。
(4)参加反应②的物质为ZnSO4和_____(填化学式)。
(5)气体M如果直接排放,会造成的大气污染,气体M为_____(填名称)。
(6)写出反应④的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用下列实验操作可分别完成“粗盐中难溶性杂质的去除”和“配制50g质量分数为15% 的氯化钠溶液”两个实验。
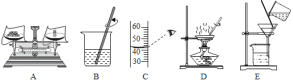
(1)操作B及操作E中玻璃棒的作用分别为______;______。
(2)C操作应选用______ 的量筒(从10mL、50mL、100mL中选择);图C中有一处明显的错误操作可能导致溶液溶质质量分数______15%(大于、小于、等于);
(3)D操作,等到蒸发皿中出现_________时,停止加热,利用蒸发皿的余热使滤液蒸干。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂的废水中含有MgSO4和FeCl3,技术人员逐渐加入NaOH溶液调节废水的pH,先后分离出两种沉淀,并通过系列处理得到有价值的产品。
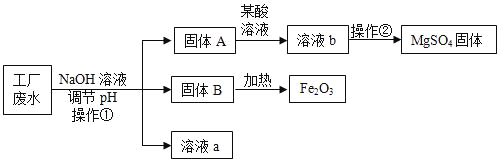
已知:Mg(OH)2、Fe(OH)3均不溶于水,加热会发生分解。分析该流程,回答下列问题:
(1)操作①的名称是_____;操作②时,当出现_____现象即可停止加热。
(2)固体A与某酸反应的化学方程式为_____。
(3)固体B加热得到Fe2O3反应前后铁元素化合价的变化情况是_____(填“升高”、“降低”或“不变”)。
(4)溶液a除了可能含有NaOH外,还一定含有的溶质有_____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纯碱、烧碱等是重要的化工原料。
(1)利用下图所示装置可间接证明二氧化碳与烧碱溶液发生了反应:将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是_____,反应的化学方程式_____。

(2)向100mL一定溶质质量分数的NaOH溶液中通入了一定量CO2,充分反应后得到溶液A,在一定条件下使溶液A中的溶质结晶析出,得到少量的白色固体。试设计实验确认该白色固体的成分。
①提出合理假设。
假设1:该白色固体为NaOH和Na2CO3;
假设2:该白色固体为只有Na2CO3;
假设3:该白色固体为_____
假设4:该白色固体为只有NaHCO3;
②基于假设1,设计实验方案进行实验,证明固体的成分是NaOH和Na2CO3。已知BaCl2溶液呈中性,请写出实验操作及预期现象和结论(下列表格中的步骤可以不填满)。限选实验试剂及仪器:蒸馏水、HCl溶液、BaCl2溶液、Ba(OH)2溶液、石蕊试液、酚酞试液、试管、胶头滴管、过滤装置。
实验操作 | 预期现象和结论 |
步骤1:_____ | _____ |
步骤2:_____ | _____ |
步骤3:_____ | _____ |
查看答案和解析>>
科目:初中化学 来源: 题型:
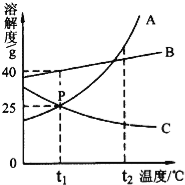
【题目】(5分)如图,A、B、C为三种物质的溶解度曲线,请根据图示信息回答下列问题.
(1)t1℃时,A、B、C三种物质中溶解度最大的是 _________ ;
(2)交点P表示t1℃时A、C两种物质的溶解度 _________ (填“相等”或“不相等”),这说明t1℃时25gA物质(或C物质)溶解在 _________ g水中能恰好形成饱和溶液.
(3)t1℃时,30gB物质投入100g水中,充分溶解,所得溶液为 _________ 溶液(填“饱和”或“不饱和”);
(4)t2℃时,A、B、C三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数的大小关系正确的是 _________ (填序号).
①A>B>C ②B>A>C ③B>A=C.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用海水晒盐的工业流程主要如下:
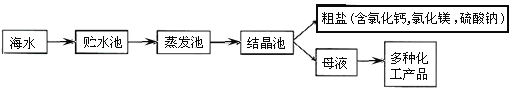
[提出问题]
怎样将析出的粗盐中含有CaCl2、MgCl2和Na2SO4都除去?
[设计实验]
方案一:工业上利用某种饱和溶液浸洗上述杂质的方法,这种饱和溶液是①________饱和溶液;
方案二:在实验室中,有人设计如下实验流程:
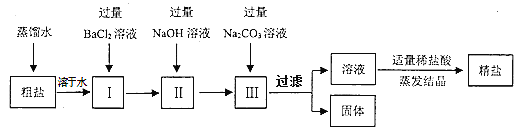
在上述方案中:
(1)在加热蒸发过程中,要用玻璃棒不断地搅拌,其目的是②__________;
(2)上述流程中,过滤出的固体成分是③__________________(写化学式);
[反思交流]
(1)通过粗盐的成分可知,其中含有Cl—和SO42-,你证明这两种混合离子的方法是:将粗盐溶于水,配成溶液,然后④__________;
(2)通过上述方法,总结检验混合离子的方法是:先选试剂,后排顺序。这里的排顺序原则是指⑤_______________;
[拓展应用]
工业上得到精盐后,用给氯化钠水溶液通电的方法制取火碱,同时还生成两种气体单质,这两种单质化合后的生成物溶于水又能得到盐酸。写出给氯化钠水溶液通电的化学方程式⑥_____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列指定反应的化学方程式正确的是( )
A. 《天工开物》烧石灰:CaCO3![]() CaO+CO2↑
CaO+CO2↑
B. 乙炔的完全燃烧:C2H2+O2![]() H2O+2CO2
H2O+2CO2
C. 稀硫酸除铁锈:2H2SO4+Fe2O3═2FeSO4+2H2O
D. 铜生锈形成铜绿:2CuO+H2O+CO2═Cu2(OH)2 CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com