
如下图所示,两个甲分子反应生成三个乙分子和一个丙分子,则从图示获得的信息中,不正确的是 ( )
| A.分子的种类在化学反应中发生了改变 | B.乙分子中含有一个A原子,一个B原子 |
| C.反应生成的丙物质属于单质 | D.该反应的反应类型为分解反应 |
B
解析试题分析:根据化学变化前后原子的种类和个数不变,结合反应的微观示意图,可推断每个乙分子是由2个A原子构成的。
A、根据反应的微观图可知,反应是由两个甲分子反应生成三个乙分子和一个丙分子,反应前后的分子构成不同,属于不同种分子,因此,反应前后分子的种类发生了改变,正确;
B、根据反应前后原子种类和个数不变,可推断乙分子由两个A原子构成,错误;
C、丙物质的分子由两个B原子构成,属于同种原子构成的分子,所以物质丙为单质,正确;
D、根据反应的微观图可知,反应是由两个甲分子反应生成三个乙分子和一个丙分子,即该反应为一种物质分解生成两种物质的分解反应,正确。故选B
考点:微粒观点及模型图的应用,单质和化合物的判别,分子和原子的区别和联系,分解反应及其应用
点评:分子是由原子构成的,且同种原子构成的分子是单质分子,不同种原子构成的分子是化合物分子。试题通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力,以检测考生从微观角度认识化学的意识和能力。


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:初中化学 来源: 题型:
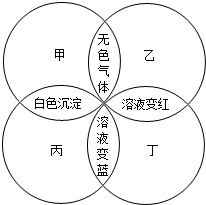 (2013?新疆)甲、乙、丙、丁分别是石蕊溶液、稀硫酸、碳酸钠溶液、澄清石灰水中的一种,若用四个圆表示四种溶液,两圆相交部分为两溶液混合后出现的主要实验现象,如下图所示.请回答:
(2013?新疆)甲、乙、丙、丁分别是石蕊溶液、稀硫酸、碳酸钠溶液、澄清石灰水中的一种,若用四个圆表示四种溶液,两圆相交部分为两溶液混合后出现的主要实验现象,如下图所示.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
(5分)在室温情况下,甲、乙、丙三种固体分别溶于两个试管和烧杯的水中,现象如下图所示,甲、丙还有剩余固体,乙固体全部溶解。升温到80℃时,发现甲固体全部溶解,乙有固体析出,丙没有明显变化。

(1)室温时,___________(选填“甲”、“乙”或“丙”)溶液可能是不饱和溶液。
(2)右图中能表示甲物质的溶解度曲线的是_______(选填“a”、“b”或“c”,下同),能表示乙物质的溶解度曲线的是_______。
(3)在t2℃时,甲、乙、丙三种物质的饱和溶液溶质质量分数由大到小的顺序是 。
(4)在温度_________时,丙物质的饱和溶液一定比甲物质的饱和溶液溶质质量分数更大。
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2011-2012学年广东省毕业生学业仿真考试化学试卷(解析版) 题型:探究题
(10分)同学们在学习碱的化学性质时,做了如下图所示的甲乙两个实验.
写出乙实验的化学反应方程式: ,反应过程中产生的现象是 .
实验结束后,甲、乙两个同学将废液倒入实验室的废液缸,结果发现废液浑浊并呈红色,他们产生了疑问.

【提出问题】废液中含有哪些物质?
【交流讨论】废液中一定含有的碳酸钙、指示剂、水和氯化钠,此外还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想:
小云认为:只有碳酸钠;
小红认为:只有氢氧化钙;
小林认为:是氢氧化钠和碳酸钠.
你认为还可能是 . (写一种猜想)
【实验设计】小方想用氯化钙溶液来验证小云、小红、小林的猜想.查阅资料获悉氯化钙溶液呈中性,设计如下实验.请你将小方的实验设计补充完整.
|
实验内容 |
预计现象 |
预计结论 |
|
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. |
①有白色沉淀,溶液呈红色. |
的猜想正确. |
|
② . |
小云的猜想正确. |
|
|
③ . |
小红的猜想正确. |
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑 .
查看答案和解析>>
科目:初中化学 来源:2011年初中毕业升学考试(内蒙古赤峰卷)化学 题型:探究题
(7分)做钠在氯所中燃烧的实验时,钠完全反应后,在集气瓶内放少量水来吸收过量的Cl2,但不能完全吸收。如何处理残余的Cl2呢?同学们进行了相关探究。
【提出问题】
向上述集气瓶中滴入石蕊溶液,发现溶液显红色。由此想到,选用氢氧化钠等碱性溶液吸收Cl2,效果会怎么样?
【查阅资料】
氯气是黄绿色有毒气体,溶于水,在饱和氯化钠溶液中的溶解度非常小。
【设计与实验】
用两套完全相同的装置做对比实验,如下图所示:
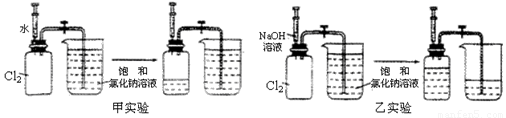
(1)为确保实验的准确性,要先检验装置的_____________________;
(2)实验开始时,先用弹簧夹夹紧乳胶管,再将注射器内等体积的水和NaOH溶液分别注入充满Cl2的集气瓶;
(3)充分吸收Cl2后,打开弹簧夹,观察进入两个集气瓶内饱和NaCl溶液的体积。
【结论与解释】
(1)甲实验中,Cl2溶于水且与水反应生成盐酸和次氯酸(HClO),反应的化学方程式为____________________________________。
(2)乙实验中,Cl2与NaOH易发生化学反应。
(3)分析实验现象得知,用碱性溶液比用水吸收Cl2的效果_________(填“好”或“差”)
【交流与反思】
(1)金属钠在氯气中燃烧的实验现象为__________________________________。
(2)向Cl2的水溶液中滴入硝酸银溶液有白色沉淀生成,化学方程式为:
_____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com