
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量样品置于试管中,加足量的水溶解,观察并用手触摸试管外壁 | 形成浊液 试管外壁发热 | 则样品中CaO 和______ 至少有一种 |
| ②将①的浊液过滤,向所得的滤液中逐滴加入氯化钙溶液至过量 | 产生白色沉淀 | 样品中含有的物质是______ |
| ③将②的浊液过滤,向所得的滤液中滴加几滴酚酞溶液 | 溶液______ | 由步骤①可知:最后滤液一定显碱性, 因此无法检验样品中的Ca(OH)2 |

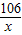 =
=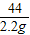 x=5.3g
x=5.3g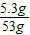 ×100%=10%
×100%=10%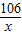 =
=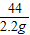 x=5.3g
x=5.3g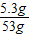 ×100%=10%
×100%=10%

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源: 题型:
已知草酸(H2C2O4)加热时在浓硫酸的作用下会发生分解反应,某化学兴趣小组对其分解产物进行了如下探究。
【提出猜想】(1)分解产物是一氧化碳和水蒸气的混合物。
(2)分解产物是二氧化碳和水蒸气的混合物。
(3)分解产物是一氧化碳、二氧化碳和水蒸气的混合物。
你认为合理的猜想是 (选填序号),依据是 。
【查阅资料】(1)浓硫酸具有脱水性,可以将有机物中的氢、氧元素按水的组成脱去。
(2)白色的无水硫酸铜遇水会变为蓝色。
(3)碱石灰是固体氢氧化钠和氧化钙的混合物。
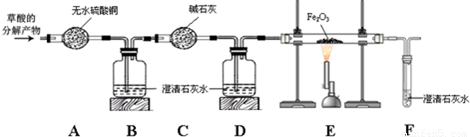
【进行实验】为了检验草酸的分解产物的成份,该小组同学将草酸的分解产物通过下图所示的装置(部分夹持仪器已略去)。

(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊,证明草酸分解产生了 。(2)装置D的作用是 。
(3)证明草酸分解产生了一氧化碳的现象应包括 。 ;装置E中发生反应的化学方程式为 。
【得出结论】草酸分解的化学方程式为 。
【反思与评价】从环保角度考虑,上述实验的不足之处是 。
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省扬州市仪征三中(学区分校)九年级(下)第十八周周末作业化学试卷(解析版) 题型:解答题

查看答案和解析>>
科目:初中化学 来源:2012年江苏省南京市白下区中考化学二模试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com