
【题目】化学用语是学习化学的重要工具。
(1)用化学符号表示:
①2个氮原子 ;
②4个氨分子 ;
③亚铁离子 ;
④氧化铝中铝元素的化合价 。
(2)用字母序号填空:
A.硫酸铜
B.聚乙烯
C.干冰
D.氧化钙
E.氢气
F.碳酸钠
①配制波尔多液的一种盐 ;
②用于包装食品的是 ;
③侯德榜制得的“碱” ;
④用作食品干燥剂的是 ;
(3)写出下列反应的化学方程式:
①铁丝在氧气中燃烧 ;
②湿法冶金 ;
③稀硫酸除去铁锈 ;
④肼(N2H4)完全燃烧生成氮气和一种常见的液体 。
【答案】(1)2N、4NH3、Fe2+、![]() (2)A 、B、F、D (3)见解析
(2)A 、B、F、D (3)见解析
【解析】
试题分析:(1)根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字即2N;化学式表示分子个数,表示多个该分子,就在其好化学式前加上相应的数字即4NH3;;根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字即Fe2-;根据O元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后即![]()
(2) 配制农药波尔多液要用熟石灰和硫酸铜, 配制波尔多液的一种盐为A;聚乙烯对人体无害,常用包装食品的塑料;侯德榜制得的“碱”为纯碱;氧化钙 常为干燥剂。
(3)铁丝在氧气中燃烧的反应物是铁和氧气,生成物是四氧化三铁,反应条件是点燃即3Fe+2O2![]() Fe3O4
Fe3O4
湿法冶金炼铜就是铁和硫酸铜溶液反应,生成硫酸亚铁和铜Fe+CuS04=Cu+FeSO4
稀硫酸除去铁锈(氧化铁)反应生成硫酸铁和水即3H2SO4+Fe2O3=Fe2(SO4)3+3H2O
肼(N2H4)完全燃烧生成氮气和一种常见的液体即N2H4+O2![]() =N2+2H20
=N2+2H20


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】绍兴市获得2015年度全省“五水共治”工作优秀市并被授予大禹鼎,“五水共治”是指治污水、防洪水、排涝水、保供水、抓节水,还社会一个蓝天碧水,为百姓创造美好的生活环境。
某化工厂流程会产生澄清废水,其中可能含有的离子是Ag+、Cu2+、Cl﹣、NO3﹣,已知:白色的沉淀Fe(OH)2在空气中会迅速转化为红褐色的Fe(OH)3。
(1)取少量废水,加入过量稀盐酸,产生白色沉淀;再加入过量氢氧化钠溶液,产生蓝色沉淀。该废水中含有的金属离子是 。
(2)兴趣小组设计了一个除去该废水中原有金属离子的实验方案,部分流程如图所示。
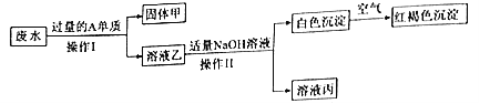
操作I的名称是 ,单质A是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成。为探究其组成(友情提示:NaCl、BaCl2溶液呈中性),进行了以下实验:

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含 。可能含有 。
(2)生成白色沉淀的化学方程式为 。
(3)无色滤液中呈碱性的物质可能含有Na2CO3;NaOH;NaOH和Na2CO3。
实验证明如下:
实验步骤 | 实验现象 | 实验结论 |
①取无色滤液少许于试管中,滴加过量的BaCl2溶液 | 产生白色沉淀 | 无色滤液中含有 |
②在①反应后的试管中滴加 | 溶液变为红色 | 无色滤液中含有Na2CO3、NaOH |
(4)白色粉末的成分是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一密闭容器中充满空气,经测定其中氮气的体积为100mL,则其中氧气的体积约为( )
A. 20mL B. 35mL C. 40mL D. 25mL
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属镁是一种重要的金属。小明在做镁带燃烧实验时,发现从实验室中取出来的镁条表面呈灰黑色,这灰黑色物质是什么呢?是氧化镁吗?小明想了一下,很快就把它否定了,他的理由是 。小明通过查阅资料灰黑色固体为碱式碳酸镁。
【查阅资料】1.碱式碳酸镁有多种组成。如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、等,可以表示为xMgCO3·yMg(OH)2(x、y都是正整数)。
2.MgCO3![]() MgO +CO2 ↑ ;Mg(OH)2
MgO +CO2 ↑ ;Mg(OH)2![]() MgO +H2O
MgO +H2O
3.碱式碳酸镁能与盐酸反应生成氯化镁、二氧化碳和水。
Ⅰ.确定镁带表面碱式碳酸镁的成分
小明同学为确定镁带表面碱式碳酸镁的组成,设计如图所示的实验:
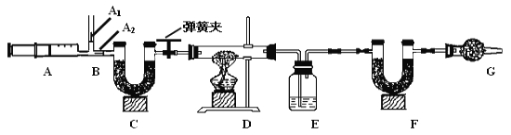
图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭。
【实验步骤】
①按图组装好仪器后, ;
②称取灰黑色样品,并将其放入硬质玻璃管中;
③打开弹簧夹,反复推拉注射器;
④称量E、F的质量,E的质量为87.6g,U型管F的质量为74.7g;
⑤关闭弹簧夹,加热D处试管直到反应不再进行;
⑥打开弹簧夹,再次反复缓缓推拉注射器;
⑦再次称量E、F的质量,E的质量为89.4g,U型管F的质量为87.9g。
【问题讨论】
(1)补充好实验步骤 ,E中所装药品是 ;
(2)C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是 ,若没有G装置,则测定的x的值会 (填“偏大”、“偏小”、“无影响”);
(3)步骤⑥目的是 ;
(4)根据上述实验数据,推算该碱式碳酸镁的化学式为 。
Ⅱ.测定镁带样品纯度
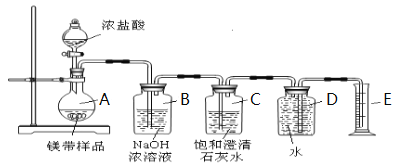
【问题讨论】
(5)装置B的作用是 ,装置C的作用是 ;
(6)称取1.0g镁带样品与足量浓盐酸充分反应后,收集到的氢气的体积为0.448 L(已知该实验条件下氢气的密度为0.089g/L),计算镁带样品纯度(写出计算过程,2分)
(7)有同学认为用这种方法测定的结果一定偏大,原因是 ;
(8)小江同学认为测定产物中CO2的质量(即反应前后装置②的质量差)也可测定样品中单质镁的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果偏低,你认为原因可能是 。(填序号)
①浓盐酸易挥发,产生的氯化氢气体被装置
②二氧化碳气体逸出时带出的水蒸气在装置B中冷凝而被吸收
③装置A、B内空气中的二氧化碳被装置B吸收
④实验结束时烧瓶中残留二氧化碳
⑤气体从氢氧化钠溶液中逸出时带走部分水蒸气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图①、②是钙元素、碘元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
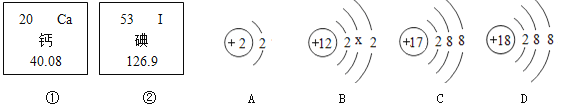
请回答:
(1)钙元素的相对原子质量为 ,碘元素为 元素(填“金属”或“非金属”)。
(2)图B中x= 。
(3)A、B、C、D中属于离子的是 (填离子符号)。
(4)钙原子的化学性质与A、B、C、D粒子中 (填字母)的化学性质相似。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国南海蕴藏着极为丰富的资源,在经济、国防上有重要意义。南海诸岛自古以来就是我国领土,我们要坚决捍卫在南海的主权。
(1)我们的食用盐大部分来自于海水,从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,可以将粗盐溶于水,然后进行如下操作:
① 过滤
② 加过量的Na2CO3溶液
③ 适量的盐酸
④ 加过量的Ba(OH)2溶液
⑤ 蒸发。
正确的操作顺序是 (填序号)。
(2)烧碱和氯气是重要的化工生产原料,我们可以利用海水为原材料大量制取。发生反应的化学方程式为:2NaCl + 2 A![]() 2 NaOH+ Cl2↑+H2↑, 则 A的化学式为 。
2 NaOH+ Cl2↑+H2↑, 则 A的化学式为 。
(3)如图是氯化钠、氢氧化钠两种固体物质的溶解度曲线。
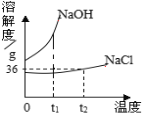
① t1℃ 时,NaOH饱和溶液的溶质质量分数 NaCl饱和溶液的溶质质量分数(填“大于”、“小于”、“等于”之一)
② t2℃ 时,将 20gNaCl固体投入 50g水中,充分溶解后可得到NaCl的 (填“不饱和溶液”或“饱和溶液”之一),此时所得溶液的质量是 g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列变化一定属于化学变化的是 ①变色 ②发光 ③燃烧 ④爆炸 ⑤铁生锈 ⑥工业制氧气⑦绿色植物通过光合作用获得氧气
A.全部 B.③⑤⑦ C.①②⑤⑦ D.除⑥以外
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com