
【题目】科学探究Ⅰ:某同学用稀盐酸和石灰石(杂质不与稀盐酸反应,也不溶于水)反应制取二氧化碳并验证其性质(如图所示),实验时发现烧杯中澄清石灰水先变浑浊,后逐渐变澄清(提示碳酸钙能与二氧化碳、水发生反应生成碳酸氢钙,碳酸氢钙易溶于水)。

(1)甲装置中发生反应的化学方程式是____。
(2)实验开始时,乙装置中澄清石灰水没有出现浑浊现象,出现这种现象可能的原因是_____。
(3)实验结束时,甲装置溶液中的溶质除氯化钙外,还可能有__(填化学式)。
科学探究Ⅱ:化学实验小组的同学在实验室里发现桌上有瓶敞口放置已久的NaOH溶液,他们对溶质的成分产生了探究的欲望。
(查阅资料)Ca2+和OH-在水溶液中不能大量共存
(提出问题)这瓶NaOH溶液一定变质了,其变质程度如何呢?
(提出猜想)猜想一:NaOH溶液部分变质;猜想二:NaOH溶液完全变质
(实验探究)
(1)氢氧化钠溶液变质的原因为_________(用化学方程式表示)。
(2)小华设计了如下实验进行探究,请根据表中内容填写:
实验步骤 | 现象 | 结论 | |
步骤一 | 取少量NaOH溶液样品于试管中,向其中滴加过量的CaCl2溶液 | 产生白色沉淀 | 猜想____成立 |
步骤二 | 过滤,向滤液中滴加酚酞溶液。 | 酚酞溶液变红 | |
如果步骤一中白色沉淀由两种物质组成,则两种物质是:________(填化学式);步骤二中根据酚酞溶液变红这一现象证明样品中含有____(填字母)。
A CaCl2 B Na2CO3 C NaOH D Na2CO3和NaOH
(实验反思)
(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液,③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代步骤一中CaCl2溶液的是____(填序号)。
(2)步骤二中用另外一种试剂代替酚酞溶液也能得出同样的结论,发生反应的化学方程式_____。
【答案】![]() 二氧化碳气体中混有氯化氢气体 HCl CO2+2NaOH=Na2CO3+H2O 猜想一 CaCO3、Ca(OH)2 C ③④
二氧化碳气体中混有氯化氢气体 HCl CO2+2NaOH=Na2CO3+H2O 猜想一 CaCO3、Ca(OH)2 C ③④ ![]()
【解析】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,盐酸和氢氧化钙反应生成氯化钙和水,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,硫酸铜和氢氧化钠生成氢氧化铜和硫酸钠。
科学探究Ⅰ:
(1)甲装置中发生反应是碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是![]() 。
。
(2)浓盐酸具有挥发性,挥发出的氯化氢和氢氧化钙反应生成氯化钙和水,实验开始时,乙装置中澄清石灰水没有出现浑浊现象,出现这种现象可能的原因是二氧化碳气体中混有氯化氢气体。
(3)实验结束时,甲装置溶液中的溶质除氯化钙外,还可能有过量的氯化氢,化学式为HCl。
科学探究Ⅱ:
[实验探究]
(1)氢氧化钠溶液变质的原因是氢氧化钠和二氧化碳反应生成碳酸钠和水,反应的化学方程式为CO2+2NaOH=Na2CO3+H2O。
(2)氢氧化钠溶液显碱性,能使无色酚酞溶液变红色,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钙反应生成碳酸钙和氯化钠。
实验步骤 | 现象 | 结论 | |
步骤一 | 取少量NaOH溶液样品于试管中,向其中滴加过量的CaCl2溶液 | 产生白色沉淀 | 猜想一成立 |
步骤二 | 过滤,向滤液中滴加酚酞溶液。 | 酚酞溶液变红 | |
如果步骤一中白色沉淀由两种物质组成,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,钙离子和氢氧根离子大量共存时生成氢氧化钙,故两种物质是碳酸钙和氢氧化钙,化学式为CaCO3、Ca(OH)2;碱性溶液能使酚酞溶液变红,氢氧化钠显碱性,步骤二中根据酚酞溶液变红这一现象证明样品中含有NaOH,故选C。
[实验反思]
(1)步骤一中滴加过量氯化钙溶液的目的是证明碳酸钠的存在并除尽碳酸钠,防止碳酸钠的存在对氢氧化钠的检验造成干扰,氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,硝酸钙和碳酸钠反应生成碳酸钙沉淀和硝酸钠,氯化钠溶液和硝酸钠溶液都呈中性,可以用氯化钡溶液、硝酸钙溶液代替氯化钙溶液,氢氧化钙和氢氧化钡中都含有氢氧根离子,它们和碳酸钠反应都会生成氢氧化钠,会对原溶液中是否含有氢氧化钠的检验造成干扰,不能用氢氧化钙溶液和氢氧化钡溶液代替氯化钙溶液,故选③④。
(2)步骤二中用硫酸铜代替酚酞溶液也能得出同样的结论,发生反应是硫酸铜和氢氧化钠生成氢氧化铜和硫酸钠,反应的化学方程式为![]() 。
。


 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:
【题目】科学实验中要研究纯净物的组成、结构、性质等,常常需要把混合物进行除杂、分离和提纯等。
(1)除去二氧化碳气体中的水蒸气,可选用的试剂是______________(写名称)。
(2)为了将氯化钠和氯化钙两种固体混合物分离,设计了下列实验方案:
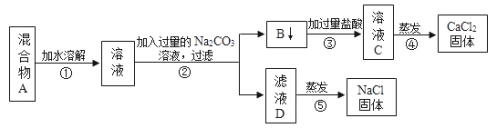
试回答下列问题:
①操作②中加入过量Na2CO3的目的是_______________,发生反应的化学方程式为__________。
②甲同学认为,上述所得的NaCl固体不纯,要得到较纯净的NaCl固体,需增加一步实验,他的做法是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水与人类的生活和生产密切相关,请回答下列问题:
(1)电解水实验揭示了水的组成。如图1实验中得到氧气的试管是_____(填“1”或“2”)
(2)自来水厂净水过程中用到活性炭,其作用是_____。
(3)海水淡化可缓解淡水资源匮乏的问题,如图2为太阳能海水淡化装置示意图。
①水变成水蒸气的过程中,不发生变化的是_____(填字母序号)
A 分子质量 B 分子种类 C 分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量分数会_____(填“变大”、“变小”或“不变”)
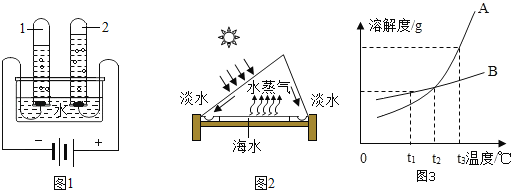
(4)如图3是A、B两种物质的溶解度曲线,根据图示回答问题:
①t1℃时,A、B两种物质的溶解度是A_____B(填“>”、“<”或“=”,下同)。
②将t3℃的A、B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A_____B。
(3)t2℃时,100g水中溶解50gA刚好饱和,那么50g水中溶解_____gB也刚好达饱和,此时溶液的质量分数是_____(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图4信息判断,下列叙述不正确的是
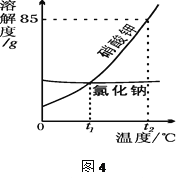
A. 硝酸钾的溶解度随温度升高而增大
B. t1 ℃时,氯化钠和硝酸钾的溶解度相同
C. 将t2℃时的硝酸钾饱和溶液降温到t1℃,有晶体析出
D. t2 ℃时,80g硝酸钾溶于100g水中可制得饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是( )

A. t1℃时,a、c两种物质饱和溶液的溶质质量分数为20%
B. 将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法
C. 将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c
D. 将150g a物质的饱和溶液从t3℃降温至t1℃,可析出30g a物质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】三位科学家成功利用高品质的氮化镓晶体作为蓝色LED光源的基础材料,开启人类照明的新时代,制造出功能强大的激光打印机、液晶电视、电脑和智能手机等。图1是元素周期表中镓元素的信息,图2是镓原子的结构示意图,回答问题:

(1)镓元素属于__(填“金属”或“非金属”)元素,在化学反应中,镓原子容易__(填“得到”或“失去”)最外层电子形成阳离子,则镓离子的化学符号为______。
(2)氮化镓(GaN)传送光线而不会将能量以热的形式浪费掉,可将手机的信号放大10倍,让电脑的速度提高1万倍。氮化镓中氮元素化合价为-3价,则镓元素的化合价为_____。
(3)传统的氮化镓制备方法是采用GaCl3与氨气(NH3)在一定条件下发生反应,则该反应的化学方程式为______________。
(4)蓝色LED因蓝光的波长短,可应用到哪些电子产品领域?_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可以用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑铜中的其它杂质)。将30ml稀盐酸分别加入到10g黄铜粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | 0.08 | 0.04 |
(1)从上表数据分析,小华用10g合金粉末共收集到氢气 g;
(2)求该合金中铜的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】目前人类正面临着石油短缺、油价上涨的严重挑战,能源紧缺问题是当今世界日益关注的热点之一,探求能源利用的新途径是人类亟待解决的重要课题。
(1)化石燃料是人类获得能量的主要来源,也是不可再生的能源,其中的一种化石能源是____,化石燃料燃烧产生的空气污染物中的一种是_______。从环保角度看,汽油和乙醇相比,较理想的燃料是________。
(2)科学家们不断研发出新能源。“神舟六号”载人飞船的运载火箭所用的高能燃料是偏二甲肼(化学式为C2H8N2),在点燃的条件下,它与N2O4反应生成氮气、水和二氧化碳。则该反应的化学方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用“碳捕捉”技术将CO和CO2混合气体的CO2捕捉并回收CO,其基本过程如图所示(部分条件及物质示未标出):
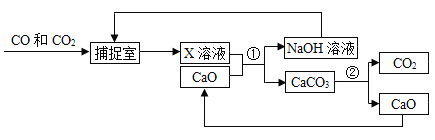
(1)反应②分离出的CO2可制成干冰,干冰常用于_________;
(2)“捕捉室”中发生反应的化学方程式为___________;
(3)反应①在“反应分离室”内进行.将NaOH溶液与CaCO3分离的操作是____________
(4)下列有关该捕捉过程的叙述正确的有_____________(填序号)
A捕捉到的CO2可制备其它化工产品,减少了温室气体排放
B“反应分离室”中的反应要吸收大量热
C整个过程中,只有一种物质可循环利用
D能耗大是该捕捉技术的一大缺点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com