
【题目】如图是甲、乙两种物质的溶解度曲线,请结合如图回答问题:
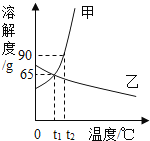
(1)_____℃时,甲、乙两种物质的溶解度相等.
(2)溶解度随温度升高而降低的物质是_____(填“甲”或“乙”).
(3)可使甲物质从其饱和溶液中结晶析出的方法是_____.
(4)t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,甲溶液的溶质质量分数_____(填“大于”、“等于”或“小于”)乙溶液的溶质质量分数.
【答案】t1 乙 降温结晶 大于
【解析】
解:
(1)由图中甲乙两物质的溶解度曲线可以知道,在t1℃时,甲、乙物质的溶解度曲线相交于一点.所以,t1℃时,甲物质的溶解度等于乙物质的溶解度;
(2)由图可知:乙的溶解度随着温度的升高而降低;
(3)甲的溶解度随着温度的升高而增大,随着温度的降低而减小,故要使甲从其浓溶液中析出,通常可采用降低温度的方法;即降温结晶;
(4)t2℃时,甲种物质的溶解度为90g>65g,乙种物质的溶解度小于65g;分别将甲、乙两种物质的饱和溶液降温到t1℃,同质量的甲、乙两种物质的溶液所含溶质质量不同,甲大于乙;所以甲溶液的溶质质量分数大于乙溶液的溶质质量分数。


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:初中化学 来源: 题型:
【题目】构建知识网络能帮助我们理解知识间的内在联系。请分析以下知识网络图,回答有关问题。
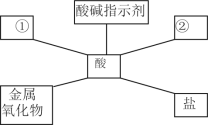
(1)①中填写_______, ②中填写_________。
(2)若酸为稀盐酸,请用相应化学方程式对①、②各举例:_____、______,上述反应类型为__、___。
(3)上图中“金属氧化物”若为氧化铁,请你写出稀硫酸与氧化铁反应的化学方程式:____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学语言包括文字语言、符号语言等。
(1)请按要求书写化学式并标出各元素的化合价:
①由地壳中含量最多的金属元素组成的氧化物_____;②紫红色的金属_____;
(2)写出下列反应的化学方程式:
①甲烷燃烧_____;
②实验室制二氧化碳_____;
③通电分解水_____;
④稀盐酸除铁锈_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铅蓄电池在生产、生活中使用广泛。其构造示意图如图,回答下列问题:

①铅蓄电池充电时是将电能转化为_____能。
②铅蓄电池放电过程中,反应的化学方程式为Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断_____(填“增大”、“减小”或“不变”)。
③稀释浓硫酸时必须非常小心,正确的操作是_____。
④废硫酸直接排放会污染环境,可以用熟石灰中和硫酸,写出该反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年11月20日,哈尔滨市滨北线松花江公铁两用桥通车了。下层为滨北线铁路桥梁,上层为市政桥梁,该桥实现二环与江北之间快速交通功能。下列相关说法不正确的是( )

A. 该桥的建成缓解了城市交通,过江开车只需5分钟
B. 桥面上铺设了特种沥青,沥青是石油炼制的产品
C. 建设该桥时用到大量的钢材,钢的含碳量比生铁高,硬度更大
D. 铺设的钢轨为韧性好、硬度大的锰钢,其主要成分为铁、锰和碳
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室现有稀盐酸、高锰酸钾、氯酸钾、大理石、紫色石蕊试液、火柴、棉花及下列仪器等(如图1所示)。
请回答:
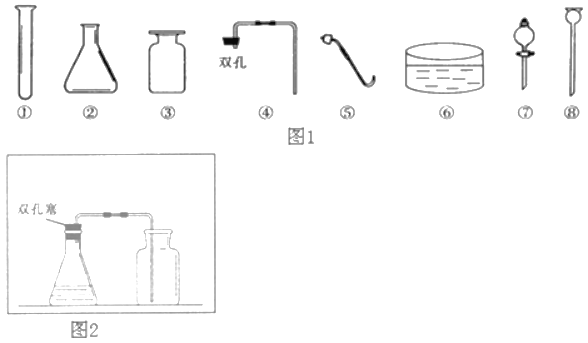
(1)若补充仪器①_____,并利用上述部分仪器和药品可以制取一种气体,其发生反应的化学方程式为②_____。收集完该气体停止加热时,应先③_____,否则因试管中温度④_____,气压变⑤_____,可能⑥_____,使试管因骤冷而炸裂。
(2)上述仪器和药品也可以制取二氧化碳。图2是小亮绘制的实验室制取二氧化碳的装置图,请你帮他补充完整①_____.若将制得的二氧化碳通入盛有紫色石蕊试液的试管中,可以观察到试管中产生的现象是②_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校课外兴趣小组用6g含少量CO2的CO的混合气体还原某二价金属氧化物RO实验,实验装置如图,数据记录如下表。已知:CO还原RO,生成金属R和二氧化碳,且装置中每个反应都充分进行,冷却C装置过程中不考虑金属R重新氧化。
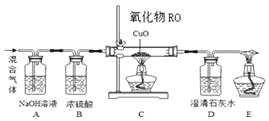
实验记录表:
实验装置代号 | A | B | C | D |
实验前药品质量(g) | 70 | 70 | 11.6 | 70 |
实验后药品质量(g) | 71 | 70.5 | 10 | 74.4 |
请分析计算:
(1)6g混合气体中CO2的质量是_____克。
(2)参加反应的CO的质量是多少_____?
(3)实验结束后,对装置C中的10g药品进行测量,测得其中R元素的质量分数为92.8%,请你求出金属R的相对原子质量_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】葡萄酒常用焦亚硫酸钠(Na2S2O5)作防腐剂。某研究小组采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置II中有Na2S2O5晶体析出,发生的反应:Na2SO3+SO2=Na2S2O5。
查阅资料:①SO2与CO2类似,能与水、NaOH溶液反应。
②亚硫酸(H2SO3)类似碳酸不稳定,易分解。
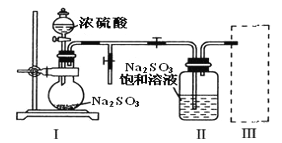
(1)装置I中Na2SO3和硫酸发生复分解反应产生SO2气体的化学方程式为_______。
(2)将装置II中析出的晶体从溶液中分离出来的操作名称是____________。
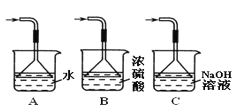
(3)装置III用于处理尾气SO2,可选用图中最合理装置为_______(填编号)。
(4)Na2S2O5溶于水即生成NaHSO3。证明NaHSO3溶液呈酸性,可采用的实验方法是_______(填编号)。
a.加入盐酸b.加入酚酞溶液c.测定溶液的pH
(5)测定某葡萄酒中防腐剂的残留量(以SO2计算)的原理:
I2+SO2+2H2O=H2SO4+2HI,利用消耗的I2量可求SO2量。在实验过程中,若有部分HI变为I2,则测定结果_______(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com