
【题目】酸、碱、盐是有广泛用途的重要化合物。某化学兴趣小组的同学围绕这几类化合物进行了一系列的探究活动。
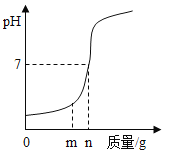
(1)用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示。熟石灰与盐酸反应的化学方程式为_____;当加入熟石灰mg时,溶液中的溶质为_____。
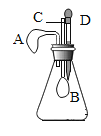
(2)设计的趣味小实验装置如图所示,其中A、B为未膨胀的气球,C为玻璃导管,D为胶头滴管。用气密性良好的该装置分别进行甲、乙两组实验。实验时均把胶头滴管中的溶液(足量)加入到锥形瓶中,并轻轻振荡。请填写下表中的空白:
锥形瓶中的物质 | 胶头滴管中的物质 | 观察到气球(A、B)的变化 | 有关反应的化学方程式 | |
甲 | 二氧化碳 | 浓氢氧化钠溶液 | _____ | _____ |
乙 | _____ | _____ | A气球胀大,B气球无明显变化 | _____ |
(3)某工厂实验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少_____?
【答案】2HCl+Ca(OH)2=CaCl2+2H2O CaCl2、HCl A气球无明显变化,B气球胀大 CO2+2NaOH=Na2CO3+H2O 二氧化锰 过氧化氢溶液 2H2O2![]() 2H2O+O2↑ 7.35g
2H2O+O2↑ 7.35g
【解析】
(1)氢氧化钙和盐酸反应能生成氯化钙和水,反应的化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;当加入熟石灰mg时,溶液的pH小于7,溶液显酸性,盐酸有剩余,溶液中的溶质是盐酸中的氯化氢和反应生成的氯化钙.
故答案为:Ca(OH)2+2HCl=CaCl2+2H2O;CaCl2和HCl;
(2)二氧化碳能与氢氧化钠反应生成碳酸钠和水,气体被消耗从而锥形瓶内的压强变小,故会观察到A气球无明显,B气球胀大,故填:A气球无明显变化,B气球胀大;2NaOH+CO2═Na2CO3+H2O;
A气球胀大,B气球无明显变化,说明锥形瓶内的气压变大,则是物质间反应产生了气体,故锥形瓶内的物质可能是二氧化锰,胶头滴管中的物质是过氧化氢溶液,过氧化氢在二氧化锰的催化作用下反应生成水和氧气,故填:二氧化锰;过氧化氢溶液;2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)设一定量石油产品中硫酸的质量为x.
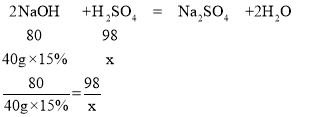
解得x=7.35g.
答:此一定量的石油产品里硫酸的质量是7.35g。


科目:初中化学 来源: 题型:
【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。在化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠与稀硫酸混合,充分反应后,有气体逸出,该反应的化学方程式为![]() ,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外,可能还含有其他成分,因此进行了猜想并做了如下实验:
,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外,可能还含有其他成分,因此进行了猜想并做了如下实验:
[实验用品] pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液
[猜想与假设]反应后溶液中溶质的可能组成成分
猜想一:硫酸钠;
猜想二:硫酸钠、碳酸氢钠;
猜想三: 硫酸钠、硫酸
[实验探究]同学们取反应后的物质用不同方案进行如下实验,请根据结论完成下表:
实验方案 | 实验操作 | 实验现象及解释 | 实验结论 |
A | 向反应后的溶液中滴加稀硫酸 | 无气体放出 | 猜想二不正确 |
B | 向反应后的溶液中滴加氯化钡溶液 | 产生白色沉淀, 其反应的化学方程式为_______ | 猜想三正确 |
C | 用镊子取一片pH试纸浸入反应后的溶液中 | 试纸变色,对照标准比色卡,PH___________7 | 猜想三正确 |
D | 向反应后的溶液中加入锌片 | ________ | 猜想三正确 |
[得出结论]猜想三正确。
[评价反思]
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显的错误操作:_____________。
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由:______。
[总结提高]依据所给实验用品,设计不同的方案确认猜想三是正确的。请写出你的实验方案的化学方程式_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图示实验中能够达到实验目的的是( )
A.测量空气中氧气质量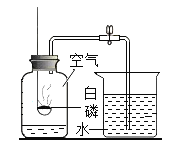
B.探究氢氧化钠与二氧化碳反应
C.检验铵态氮肥
D.区分氢氧化钠、氯化钠、碳酸钠溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科。根据图回答问题:
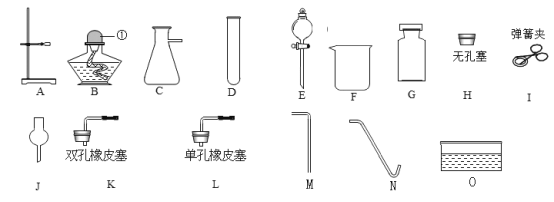
(1)写出仪器的名称:①_____________②_______________。
(2)实验室选用B、D和_____________(填字母)可组装成一套实验室制取并收集较纯净氧气的装置,涉及的化学方程式为_____________。
(3)如果用H和____________ (填字母) 可组装成一套制备气体的发生装置,用该装置可适合下列实验室制备的气体有____________(填字母) ;
A 用高锰酸钾制O2
B 用锌和稀硫酸制H2
C 用石灰石和稀硫酸制CO2
(4)实验室制备二氧化碳气体的装置要能达到“随开随用,随关随停”,可选用上述的仪器_____________(填字母)组装;
(5)实验室用电石(主要成分CaC2)和水反应制取乙气体炔(C2H2)气体和另一种化合物,该反应的化学方程式是____________。用电石制得的乙炔气体中常混有酸性气体,为了得到较纯净的C2H2, 可将气体通过_____________,溶液后,用排水法收集,请在如图将除杂及收集装置补画完整_____________。
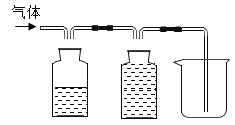
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。则t2℃时,甲的溶解度等于_____g;t1℃时,20g乙物质投入100 g水中,充分溶解,所得溶液为_____ ( 选填“饱和”或“不饱和”)溶液; t2℃时,将甲、乙、丙三种物质的饱和溶液降温到t1℃,所得溶液中溶质质量分数的大小关系是_____。
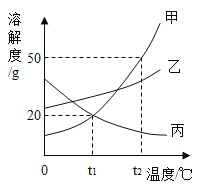
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1是实验室制取氧气或二氧化碳时经常用到的仪器,请回答有关问题。
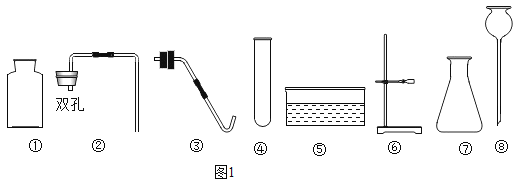
(1)写出仪器的名称:⑧_____。
(2)当制取较多量CO2时,制取装置的仪器组合是_____(填序号),化学方程式是_____。
(3)阅读材料,回答问题:
①氨气是有刺激性气味的无色气体,密度比空气的小,极易溶于水,其水溶液显碱性。
②加热熟石灰和氯化铵的固体混合物生成氨气。
③湿润的红色石蕊试纸遇到氨气变成蓝色:氨气遇到浓盐酸时产生白烟(生成NH4Cl固体)。
Ⅰ.制取氨气的装置与实验室用_____(填“高锰酸钾”或“过氧化氢溶液”)制氧气的装置相同。
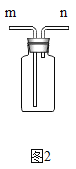
Ⅱ.若用图2所示装置收集氨气,进气口应为_____(填“m”或“n”)端,检验氨气是否收集满的方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线。下列叙述正确的是
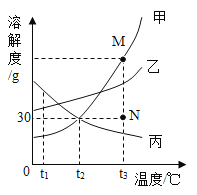
A.t1℃时, 等质量的甲、乙溶液中所含溶质的质量为乙>甲
B.t2℃时,20g 丙能溶解于50g水中形成70g溶液
C.若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D.将t3℃时甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲=丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙炔是一种常见的有机燃料,将乙炔在纯氧气中燃烧后进行以下实验,已知①含碳元素的物质完全燃烧形成CO2,不完全燃烧生成CO;②白色无水CuSO4粉末遇水变蓝色:
(1)若选用过氧化氢溶液和二氧化锰来制取纯氧气,为控制反应速率应选下面发生装置中的__________(填序号)。
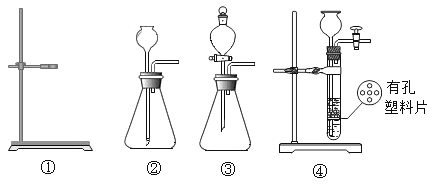
(2)将燃烧的产物依次通过A-F装置(部分夹持、固定装置省略)进行验证:若交换A、B装置的后果是___________________________。
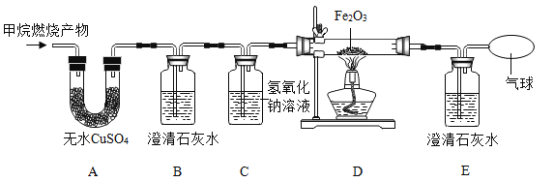
(3)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水均变浑浊,D中红色粉末变成黑色,由此推断该实验中乙炔燃烧的产物是____________,实验过程中除去CO2的反应的化学方程式是_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有人提出工业生产回收利用空气中CO2的构想:把空气吹入浓碳酸钠溶液中,溶液可吸收CO2生成碳酸氢钠(NaHCO3);加热碳酸氢钠固体又分解放出CO2;在合成塔内CO2与氢气反应生成甲醇(CH3OH)和水。简要的生产流程如图所示:
(图中:“→”表示流程顺序或步骤,“↓”表示加入原料,“↑”表示生产出得产物,“ ![]() ”表示有可循环利用的物质)
”表示有可循环利用的物质)

【资料卡片】碳酸氢钠分解温度是270℃,碳酸钠在856℃熔化,但还未达到分解温度。
请回答下列问题:
(1)大气中CO2浓度不断增大的人为原因是____;由此引发的环境问题是______(填序号)
A、酸雨 B、温室效应 C、臭氧空洞
(2)吸收池中发生反应的化学方程式________________;
(3)合成塔中发生反应的化学方程式________________;
(4)该流程中能循环利用的物质是__________________(写出一种即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com