
����Ŀ��̼��������FeCO3������ȡ��Ѫ����ԭ�ϣ��������û�ͭ���Һ[���ʳɷ�ΪFe2��SO4��3��CuSO4��H2SO4]Ϊԭ�ϣ��Ʊ�̼������������ͭ����������ʾ��ͼ��
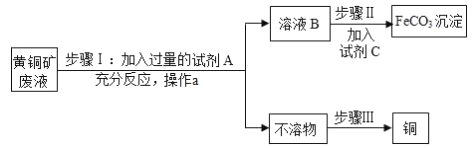
��֪����Fe��Fe2��SO4��3��Һ�ܷ�����Ӧ����FeSO4����ҺB��ֻ��һ�����ʡ�
��1������1�У��Լ�AΪ_____���������A��Ŀ����ʹ��Һ��Fe2��SO4��3��CuSO4��H2SO4ȫ��ת��Ϊ_____����Ӧ�����й۲쵽������֮һ���к�ɫ����������д���÷�Ӧ�Ļ�ѧ����ʽ_____��
��2������a�����ƣ�_____��
��3��������У��Լ�C�Ļ�ѧʽ����Ϊ_____�ȿ�����̼���Ρ�
��4��������Ŀ���ǣ���ȥ�����������е���һ�ֽ��������յõ������������ͭ���û�ѧ��������ͭ�IJ�������Ϊ�����������ϡ������ᡢ���ˡ�ϴ�ӡ��������ͭ����������Ϊ_____��
���𰸡��� FeSO4 Fe+CuSO4��Cu+FeSO4 ���� Na2CO3�ȿ�����̼���� ��������
��������
��1�����������Ʊ�̼��������ͭ������Ϊ���������µ����ʣ�����1�У��Լ�AΪ ������������
�������A��Ŀ����ʹ��Һ��Fe2��SO4��3��CuSO4��H2SO4ȫ��ת��Ϊ������������������������
��Ӧ�����й۲쵽������֮һ���к�ɫ��������������������ͭ��Ӧ��������������ͭ���ʷ�Ӧ�Ļ�ѧ����ʽдΪ�� Fe+CuSO4��Cu+FeSO4��
��2������aʵ���˹����Һ��ķ��룬�ò���Ϊ���ˣ�������ˡ�
��3���������������������Cת������̼�����������������غ㶨���Լ����ֽⷴӦ���ڷ�Ӧ�������������ɲ��ܣ������趼�ܡ��������Լ�C�Ļ�ѧʽ����Ϊ Na2CO3�ȿ�����̼���Σ�����Na2CO3�ȿ�����̼���Ρ�
��4����������������������ͭ�����Ի���ͭ����������Ϊ�����������������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�Ľ��ۻ�����в���ȷ���ǣ�������
A. ˮ�տ����װѺ��dz��𩁩�˵���¶����߷��ӻ���
B. ���Ĺ���ʱ��Ʈ�㩁��˵�������ڲ����˶�
C. ����кͷ�Ӧ��������ˮ����ʵ����H+��OH�� ���������H2O
D. Ũ�����ڿ��������ɰ�������Ũ������лӷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪA��B��C��������(�������ᾧˮ)���ܽ�����ߣ�����˵����ȷ����( )
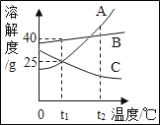
A. t1��ʱ��A��C�������ʱ�����Һ�к��е���������һ����ͬ
B. t1��ʱ��A��Һ������������Ϊ20%
C. t2����������ʵı�����Һ���µ�t1��ʱ���������������ɴ�С��˳��ΪB��A��C
D. t1��ʱ��125gA���ʵı�����Һ��ˮϡ�Ϳ��Եõ�250g��������10%��A���ʵ���Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ļ���ԭ�ϣ�Ҳ��ʵ�����г��õĻ�ѧ�Լ��������Ƕ���������ʡ���ȡ����;�ȷ����̽�������㹲ͬ���벢�ش��й����⡣
��̽��һ�����������
(1)̽��Ũ�����ijЩ���ԡ�
����Сľ��պȡ����Ũ���ᣬ����һ��ɹ۲쵽___��
��Ũ�����ϡ�ͣ�Ũ����ϡ������ͼ1��ʾ��b��ʢ�ŵ�������___��a��������___��
����ȤС���98%��Ũ����10ml��63.3%��������ҺԼ20mL�ֱ����������ͬ��С�ձ��У��������۲졢��¼���������������»�����ʵ������ݻ�ɵ�������ͼ2����ͼ2�������ܵõ���ʵ����ۣ�_____(д����)��
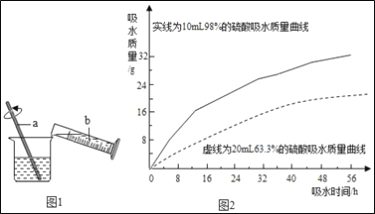
(2)̽��ϡ����Ļ�ѧ���ʡ�
��ͼ3��������ϡ����ֱ����A��E����ֻ�ձ��С�
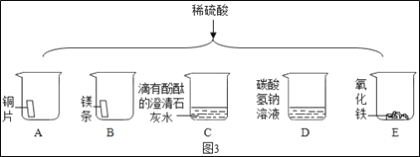
���в������ݵ���___(����ţ���ͬ)���а�ɫ�������ɵ���___��
����֤��C�з�����ѧ��Ӧ��������___��
(3)��д��ϡ�����һ����;___��
��̽����������Ĺ�ҵ�Ʒ���
��ҵ���Ի�����Ϊԭ����������Ĺ���������ͼ4��ʾ��
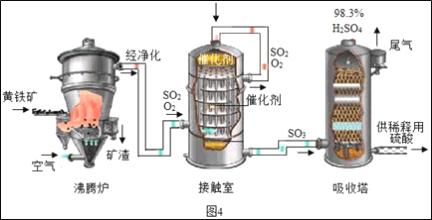
(1)�Ӵ����з����Ļ�ѧ����ʽΪ___��
(2)������������Ĺ�������ͼ������˵����ȷ����___(����ĸ���)��
A Ϊʹ��������ȼ�գ��轫����� B �����ܹ����SO2�ķ�Ӧ���ʺͲ���
C �������еõ��IJ�ƷΪ����� D ����¯�ų��Ŀ����ɹ�����
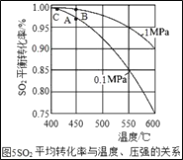
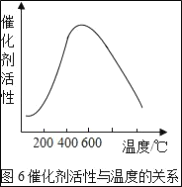
(3)�Ӵ����е�SO2ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ5��ʾ�������������¶ȵĹ�ϵ��ͼ6����ʵ�������У�SO2��������Ӧ������ѡ��ѹ��450��(��Ӧͼ��A��)����û��ѡ��SO2ת���ʸ��ߵ�B��C���Ӧ�ķ�Ӧ��������ԭ��ֱ���___��___��
��̽������̽��ij��������FeS2�ĺ�����
ͬѧ�ǽ���������ʵ��̽����
���������ϣ���4FeS2 +11O2 ![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
��Na2SO3 +H2O2 ��Na2SO4 +H2O
��ʵ��̽����
���ȡ1.60g��������Ʒ������ͼ7��ʾװ��(�г�װ��ʡ��)��ʯӢ���У���a�����ϵػ���ͨ���������������ʯӢ���еĻ�������Ʒ����ȫ��Ӧ��
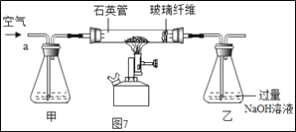
��Ӧ��������ƿ�е���Һ������ͼ8����
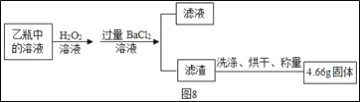
���������ۣ�
(1)I��װ�ü�ƿ��ʢ�ŵ��Լ�������������Һ����������___��II����Һ����������һ����___��
�������ⶨ��
(2)II�����յõ���4.66g������___(�ѧʽ)��
(3)����û�������FeS2����������Ϊ___��(д���������)
��������˼��
(4)���ȱ�ټ�װ�ã������ղ��FeS2��������������___(����ƫ������ƫС����������)
(5)���֤��II������BaCl2��Һ�ѹ���(���Ҫд����������������)___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������е������ʵ��ԭ����ȷ���ǣ� ��

A������ʼ�ղ�ȼ��

B��������

C��U����Һ������ҵ�

D����֤Fe��Cu��Ag�Ľ������ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�� X��Y �������Ľṹʾ��ͼ������˵����ȷ���ǣ� ��

A��X Ϊԭ�ӣ�Y Ϊ����
B��X��Y �����ڷǽ���Ԫ��
C��X �ڷ�Ӧ�п�ʧȥ 6 ������
D��X �� Y �γɻ�����Ļ�ѧʽΪ YX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ҹ���������ʳ����ʷ�ƾá�������õ�һ��ȼ���ǹ���ƾ���ij��ѧ��ȤС���ͬѧ��������ƾ��������˺��棬����ɷֽ���̽��������ش��������⡣
���������ϣ�
a������ƾ�Ҳ����Ϊ"�ƾ���"�����ȼ�Ͽ顣����ƾ������ǹ���״̬�ľƾ����ǽ��ƾ���Ӳ֬����������ư�һ���������Ȼ���Ƴɡ�
b���ƾ��Ļ�ѧʽΪC2H5OH��
c.�Ȼ������Ȼ�����Һ�������ԡ�
d. BaCl2+Na2CO3=BaCO3��+2NaCl ���ɵ�BaCO3Ϊ��ɫ����
��������⣩
(1)�ƾ��Ļ�ѧʽ��NaOH��ȣ�������OH������ô�ƾ���ˮ��Һ�Dz����Լ��ԣ�
(2)����ƾ��е����������Ƿ���ʼ����ʵij̶���Σ�
��ʵ��̽��1���ƾ���ˮ��Һ�Dz����Լ���
ͬѧ��ȡ�����ƾ���Һ���Թ��У��μ���ɫʯ����Һ��δ�۲쵽��ɫʯ���Ϊ��ɫ��˵���ƾ���Һ_______(������������������)���ԡ�
��ʵ��̽��2������ƾ��е����������Ƿ���ʼ����ʵij̶����
�ٹ���ƾ��е����������Ƿ���ʣ�ͬѧ����ȡ��������ƾ����ձ��У���������ˮ�ܽ��μ�������ϡ���ᣬ�۲쵽__________����˵�����������ѱ��ʣ���д�����������ڿ����б��ʵĻ�ѧ����ʽ______________��
��Ϊ��һ��ȷ���������Ƶı��ʳ̶ȣ��������̽����
����ͬѧȡ�ձ��ϲ���Һ����֧�Թ��У�����ͼ��ʾ����ʵ�顣
ʵ�鷽�� |
|
|
ʵ������ | ��Һ��� | ����__ |
ʵ����� | ��Һ������������ | ��Һ����̼���� |
����ͬѧ��Ϊ����ʵ�鲻��֤����Һ��һ�����������ƣ�������__��������ȡ�ձ����ϲ���Һ���������Ȼ�����Һ����ַ�Ӧ���ã�ȡ�ϲ���Һ���μӷ�̪��Һ����̪��Һ��졣
����˼����������ʵ���м������Ȼ�����Һ��Ŀ����________��
��ʵ�����]С��ͬѧ�������ۣ�һ����Ϊ�ù���ƾ��е��������Ʋ��ֱ��ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�к��зḻ���Ȼ�þ����ͼ�ǴӺ�ˮ����ȡþ�ļ����̣�����ȡMg�Ĺ����У�

��1���Լ�A���ѡ��_____�����ҹ��зḻ��ʯ��ʯ��Դ���ǣ�������B���Լ�C���������кͷ�Ӧ�������B�Ļ�ѧʽΪ_____��
��2������ˮMgCl2��ȡMg�Ļ�ѧ����ʽΪ_____��
��3����ˮ�������Ǻ���MgCl2����Һ������ͨ�������������õ���MgCl2��Һ�кβ�ͬ��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ��װ��ͼ���ش����⡣

��1��ͼ�б���a������������_____��
��2��ʵ�������������������̵Ļ������ȡ������ѡ�õķ���װ����_____������ĸ�����Թܿ���������б��ԭ��_____����Ӧ�Ļ�ѧ����ʽΪ_____��
��3��ʵ�����������п����ȡ��������Ӧ�Ļ�ѧ����ʽΪ_____������Bװ�øĽ�ΪCװ�ã���Ľ�����ŵ���_____������Eװ���ռ��������������_____�˽��루�b����c��������Ҫ��ȥ�����л��е��Ȼ��⣬��Dװ���пɷ�����Լ���_____������ĸ����
A ����������Һ B ̼��������Һ
��4��ʵ��С������ͼװ�ý�������ʵ�顣
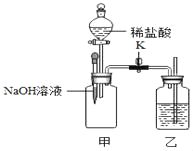
��֪����ƿ�г���������̼������Һ����ˮ��ʵ��ǰK�رա�
������ͷ�ι��е�ŨNaOH��Һ����ƿ�У����÷�Ӧ�Ļ�ѧ����ʽΪ_____��
����K���۲쵽���е��ܿ�������ð����ԭ����_____��
������Һ©���е�ϡ����ע����У��۲쵽���е�������_____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com