
| �۵� | �е� | ���ȶ��� | �����ʯ��ˮ��Ӧ |
| 101��C��102��C | 150��C��160��C���� | 100.1��Cʧȥ�ᾧˮ��175��C�ֽ��CO2��CO��H2O | ��Ca��OH��2��Ӧ������ɫ������CaC2O4�� |

���� ���ᾧ����۵�ϵͣ����������ۻ���
Ҫ��Ϥ�������������ơ���;��
��д��ѧ����ʽҪע��淶�ԣ�
�������ʵ����ʿ��Խ�����ط�����жϣ�
���ݻ�ѧ����ʽ���Լ�����ᾧ�������������
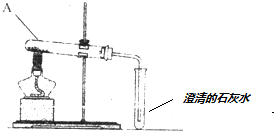
��� �⣺��1��������۵�ϵͣ����������ۻ�����cװ�ü��Ȳ���ʱ�����������������������Ȳ��ᣮ
���c��
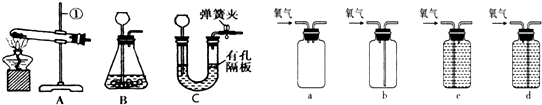
��2��������a��b�����Ʒֱ����ձ���Ӳ�ʲ����ܣ�
����ձ���Ӳ�ʲ����ܣ�
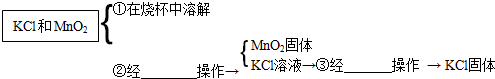
��֤������CO2�������ǣ�B�г����ʯ��ˮ����ǣ�֤������CO�������ǣ�D�к�ɫ�����ɺ�ɫ��
���B�г����ʯ��ˮ����ǣ�D�к�ɫ�����ɺ�ɫ��
D������ͭ��һ����̼�ڼ���ʱ��Ӧ������ͭ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽ�ǣ�CO+CuO$\frac{\underline{\;\;��\;\;}}{\;}$Cu+CO2��
���CO+CuO$\frac{\underline{\;\;��\;\;}}{\;}$Cu+CO2��
��װ��A�������ǣ���ȥ������������ֹ�Զ�����̼�ļ���������ţ����ҵ������ǣ��ռ�һ����̼����ֹ��Ⱦ������
�����ȥ������������ֹ�Զ�����̼�ļ���������ţ��ռ�һ����̼����ֹ��Ⱦ������
��3����һ����̼���ַ�Ӧ�����ɵ�ͭ���±����������ض��ܹ����¼������ʵ������ʵ��ֵƫ�ͣ�
������ɵ�ͭ�ֱ�������
�ڸ��������Һ����ɫ�Ϻ�ɫ�ģ�
����Ϻ죮
25.00g3.16%KMnO4��Һ��KMnO4������Ϊ��25.00g��3.16%=0.79g��
���0.79��
��10.00g��Һ�к����ᾧ�������ΪX��
��2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2��+8H2O��֪��
5H2C2O4•2H2O��5H2C2O4��2KMnO4��
630 316
X 0.79g
$\frac{630}{316}=\frac{X}{0.79g}$
X=1.575g��
50.00g��Һ�к����ᾧ�������Ϊ��1.575g��5=7.875g��
���ᾧ�����������Ϊ��$\frac{7.875g}{8.75g}$��100%=90%��
����Ʒ�в��ᾧ�����������Ϊ90%��
���� �����漰��ѧ����ʽ����д��ʵ��������жϡ����ݻ�ѧ����ʽ���м���ȷ����֪ʶ���ǵ��͵��ۺ��⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ش��й�̼�ۺ�����ͭ��Ӧ�����⣮
��ش��й�̼�ۺ�����ͭ��Ӧ�����⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʯ�����ƵIJ�Ʒ | |
| B�� | �·��ϵ����ۿ���ͨ�������ܽ����۶���ȥ | |
| C�� | ҽ����100mL������ˮ�к���0.9gҽ���Ȼ��� | |
| D�� | ����ˮ�շ���Ŀ�а���ˮ��Դ�Ѻ���ˮ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com