
����Ŀ����4������������Ȼ��ص��ܽ��������ͼ��ʾ���ش��������⣺
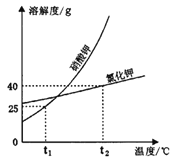
��1��t2��ʱ�������ʵĵ�����������Һ������t1�棬�������������ϴ���� ����Һ��
��2��t2��ʱ����50gˮ����ʢ��25g�Ȼ��ص��ձ��У�����ܽ�õ��Ȼ�����Һ�������� g�������¶Ȳ��䣬�����ձ����ټ���5gˮ����ֽ�����Ȼ�����Һ�����ʵ��������� �����������䡱��С������
��3����������л��������Ȼ���ʱ������ �����ᴿ�������
���𰸡���1������� ��2��70 ���� ��3����ȴ�ȱ�����Һ�������½ᾧ����
��������
����������ܽ�����¶�Ӱ�������ʣ���ͬ�ı�����Һ������ͬ���¶������ľ���࣬�ʣ�1��t2��ʱ�� �����ʵĵ�����������Һ������t1�棬�������������ϴ��������أ�(2�������Ȼ���t2��ʱ���ܽ�ȵ���ֵ��֪��50gˮ����ʢ��25g�Ȼ��ص��ձ��У�����ܽ�õ��Ȼ�����Һ��������70g�������ձ����ټ���5gˮ����ֽ�����Ȼ�����Һ�����ʵ������������䣬��Ϊ�ڼ�ˮ֮ǰ��Һ������������ʣ�࣬����ˮ�����ܽ���ʣ������ʣ���ȻΪ������Һ���������ʵ������������䡣��3����Ϊ����ص��ܽ�����¶ȵ����߶��������ʵõ�����ز��ý��½ᾧ��


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ж�þ��ȼ���ǻ�ѧ�仯����Ҫ������
A������ҫ�۵İ�
B���ų���������
C�����ɰ�ɫ��������þ
D����ɫ�ı���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ������Һ60.0g���μ���������26.5����Na2C03��Һ������ͼ������ҺpH�ı仯����ͼ��ʾ

��1����������ǡ����ȫ��Ӧʱ̼������Һ������Ϊ g��
��2��������������Һǡ����ȫ��Ӧ����Һ�е���������������д��������̣���ȷ��0��1������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4������������ȼ�������Ļ�ѧԭ���Ա��������Ʋ���ȫ�dz���Ҫ��
��1��2013��12�¹��ݽ�ҵ���÷������ػ��֣���ȼ�����������������ڴ�ŵĴ���Ь��ֽ�����Ʒ�䵱�� ��
��2���߲㽨����ͨ�����������õ���ˮϵͳ�������ԭ����������ˮ��������Ҫ�� ��
��3��������ͼ���е����ݣ��ش����⣺
���ʴ��� | L | M | N | P |
�۵�/�� | ��117 | 3550 | 44 | ��259 |
�е�/�� | 78 | 4827 | 257 | ��253 |
�Ż��/�� | 510 | 370 | 40 | 580 |
��������Ϊ�����ʵ��ۡ��е�Խ�ߣ��Ż��Խ�ߡ����ý��� ���������������������
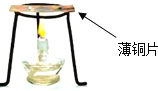
����֪�ƾ��ƻ�����¶�ԼΪ500�森������ͼװ�ã���֤�ﵽ��ȼ���Ż����ȼ�յ�����֮һ���ϱ��п�������ɸ�ʵ������ֿ�ȼ���� ��N�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ƺò������������ǽ�ڿ���ǽ���㡱������˵����
A�������ڲ�ͣ�˶� B�����Ӽ��м��
C�����Ӻ�С D�����ӿ��Էֽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3�������ͻ�β���е���Ҫ��Ⱦ���ǵ������ij��β���������������ð����뵪���������ѧ��Ӧ��������Ⱦ���ŷţ�����һ����Ӧ����ʾ��ͼ������ʾ��
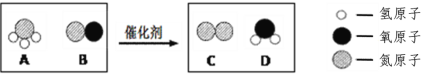
�ش��������⣺
��1��A����Ԫ�صĻ��ϼ�Ϊ ��
��2��A���ӡ�B���ӡ�C���ӵ���ͬ���Ƕ����е� ������ӡ���ԭ�ӡ���Ԫ�ء��� ��
��3���μӷ�Ӧ��A��B�ķ��Ӹ�����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Fe2O3��������������FeO����������������Fe3O4�������������������У����������������ɴ�С˳�����е���
A��Fe3O4��Fe2O3��FeO B��FeO��Fe2O3��Fe3O4
C��FeO��Fe3O4��Fe2O3 D��Fe2O3��Fe3O4��FeO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����9�֣��й����ʵ�ת����ϵ��ͼ��ʾ������X��YΪ������̬���ʣ� ZΪ�����������ʣ�AΪ����л������Ϊ��Ȼ������Ҫ�ɷ֡�B��C��DΪ�����M��һ���ж������塣

�ش��������⣺
��1��д���������ʻ�ѧʽ
C�� D�� Y��
��2����Ӧ�١��� ���ۡ��������ڻ��Ϸ�Ӧ��Ϊ ������ţ���ͬ���������û���Ӧ��Ϊ ��
��3��д����Ӧ�ٵĻ�ѧ����ʽ ��
��4����ͼ�е�dz��ɫ��Һ�������ᱵ���ɲ�����ϡ����İ�ɫ����������Ӧ���Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10��)�ҹ�������ѧ�Һ�°������������Ƽ����Ҫԭ���ǣ�I����Ũ��ˮ��ͨ��������CO2��ʹ������ˮ��CO2�������Ϸ�Ӧ������NH4HCO3��Һ��II����������Һ�м���ʳ��ϸ������ֽ��裬�������ܽ�Ƚ�С��С�մ���岢�õ�������Һ��III�����������Ĺ�����ȡ����˷�����������Ӧ���ڻ�����ҵ��ij������ҵ�Ĺ�������ʾ��ͼ���£�

�����������գ�
��1���������Ƽ�ԭ��II���з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2������ͼ�������У��ȼ�Ca��OH)2��Һ��Ŀ���� ���ټ���Na2CO3��Һ��Ŀ���� ��
��3��������1���������� ����������Һ������Һ��pH 7���������������С�������������������Ӷ�����������������A��������AΪ �������ƣ���
��4��������270������С�մ���ȫ�ֽ⣬�������Ȳ��ֽ��������ʣ���ѧ��ȤС���ͬѧ��ʵ�������������������������ʾ�ΪС�մ���������ʵ�飺��ȡ20.00g����Ĺ�����Ʒ����������300�����¼������������䣬�ڸ���������ȴ�����������������Ϊ19.38g��
������Ŀ������Ϣ���������Ʒ�д��������������д��������̣���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com