
【题目】有一含有纯碱的食盐样品,为了测定其中碳酸钠的含量,某同学称取10g的样品放入烧杯中,向烧杯中加入100g足量的 稀盐酸,充分反应后气体全部逸出,烧杯中剩余物的总质量为109.56g(假设产生的气体全部逸出。以下计算结果保留一位小数)
(1)样品中碳酸钠的含量是___
(2)NaCl中氯元素质量分数是____
(3)反应后溶液中溶质质量分数是___?
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】实验室需配制一定溶质质量分数的溶液。
(1)配制100mL质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),所需氢氧化钠的质量为_____g,所需蒸馏水的体积为_____mL(水的密度为lg/cm3)。
(2)用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要_____。
(3)下列操作正确的是_____。
A称量氢氧化钠固体时,左盘放砝码
B将准确称量的氢氧化钠固体放入装有水的量筒中溶解
C将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
D称量时,先添加所需的氢氧化钠,再移动游码直到天平平衡
(4)把10%的氢氧化钠溶液加水配制为150g质量分数为8%的氢氧化钠溶液,需水的质量为_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列装置常用于实验室制取气体,根据给出的装置回答下列问题
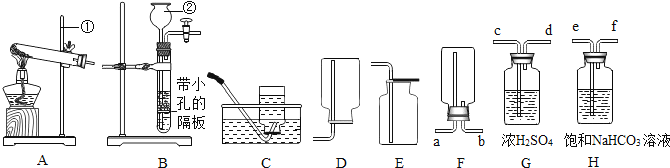
(1)指出编号仪器名称:①______;②______。
(2)实验室利用A装置用氯酸钾制取氧气,反应原理用化学方程式表示为______。用收集到的氧气完成硫粉燃烧实验后,还需向集气瓶内加入适量氢氧化钠溶液,目的是______(用化学方程式表示)。
(3)制取并收集二氧化碳应选择的装置是______(从A-E中选择),使用该套装置制取气体的突出优点是______,制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使用G、H装置将以上气体除去,则装置正确的连接顺序是:混合气体→______(用端口字母表示)
(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH______7(填“>”“<”或“=”)
(5)已知碱石灰是氧化钙和氢氧化钠的固体混合物,下列气体①氢气②氧气③一氧化碳④氯化氢⑤二氧化硫⑥氨气。不能用碱石灰干燥的是______。
A ①②③ B ④⑤⑥ C ④⑤ D ⑤⑥
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】食品与健康、能源与环境是我们共同关注的社会问题。
(1)紫薯营养丰富,具有特殊的保健功能。紫薯中富含淀粉、维生素C、维生素B、铁、钙、硒等。
①这里的“铁”“钙”是指 ______;
②人体缺“铁”,会导致______病症;
③紫薯中能给人体提供能量的物质是______;
④硒元素被誉为“抗癌大王”。硒元素的部分信息如下图。下列说法正确的是______(填序号)。
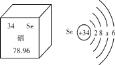
A 硒属于金属元素 B 一个硒原子中有34个质子
C 硒的原子结构示意图中x=18 D 硒元素的相对原子质量为78.96g
(2)①合理使用化肥是农业增产的重要手段,下列属于复合肥的是(填序号)______;
A 尿素[CO(NH2)2] B 硫酸钾[K2SO4]
C 磷酸二氢铵[NH4H2PO4] D 硝酸钾[KNO3]
②配制农药波尔多液时不宜用铁制容器,用化学方程式表示原因_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种物质的溶解度曲线,请回答:
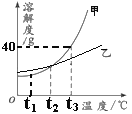
(1)t3℃时,两种物质溶解度的大小关系为甲__乙;(填“大于”、“小于”或“等于”)
(2)t3℃时,把30g固体甲放入50g水中,充分溶解后可得到甲的溶液_____g;
(3)在其他条件不变的情况下,若把t1℃时甲、乙的饱和溶液分别升温至t2℃,此时两种溶液中溶质的质量分数关系为甲__乙(选填:>、<或=)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是化学实验中常用的几种装置.
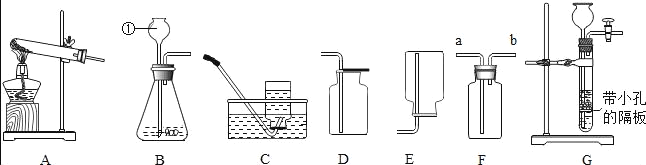
请回答下列问题:
(1)指出有编号的仪器名称:①___.
(2)写出实验室利用上述A装置制取氧气的化学反应方程式___.
(3)若用F装置干燥生成的氧气,F中盛放的液体试剂是___,气体应从___端导入(填“a”或“b”).
(4)用KClO3制氧气时需加MnO2作催化剂.若在KClO3中加少量的KMnO4,也能加快KClO3的分解.用文字说明其原因___.
(5)写出用石灰石和稀盐酸制取二氧化碳的化学方程式___,
使用G装置制取该气体的突出优点是___,收集二氧化碳气体的装置是___;检验二氧化碳集满的方法是___.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明对废弃的易拉罐很有兴趣,为测定易拉罐中铝元素的质量分数,他剪取W克镁铝合金的易拉罐,先用过量稀硫酸溶解,然后再向溶液中滴加一定量的NaOH溶液得到Al(OH)3沉淀,继续滴加NaOH溶液时Al(OH)3被溶解[已知:Al(OH)3与NaOH反应成NaAlO2和H2O].而Mg(OH)2不溶于NaOH溶液,沉淀质量与滴加NaOH溶液质量关系如图所示
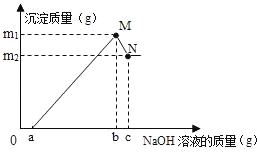
(1)写出Al(OH)3与NaOH反应的化学方程式_____;
(2)在a点时,溶液中的溶质有哪些?_____(填化学式);
(3)易拉罐中铝元素的质量分数为多少?_____(用字母表示,假定易拉罐只由镁和铝组成)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色固体可能由NH4Cl、Na2 SO4、Na2 CO3、Ba(OH)2、ZnCl2中的一种或几种组成,为确定其成分,进行了如下实验,请回答下列问题.
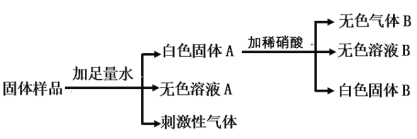
(1)刺激性气体的化学式为_____;
(2)根据流程图所示实验,能确认原白色固体中一定含有的物质是_____;
(3)取白色固体B,继续加入足量稀硝酸,若观察到仍有白色固体剩余,则产生这种剩余白色固体的反应化学方程式为_____;
(4)证明ZnCl2是否存在的实验操作为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表为部分元素的粒子结构示意图。
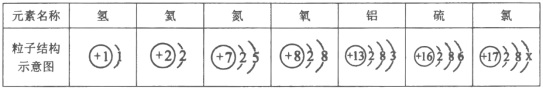
请回答下列问题:
(1)若氯原子最外层得到一个电子,其微粒符号为_______;
(2)表中具有相对稳定结构的原子是_______ (填元素符号);
(3)根据表中信息,确定一个硫化氢分子中所含电子总数为_______;
(4)将氮元素与铝元素形成的化合物放入水中,立即生成白色沉淀氢氧化铝,并放出一种有刺激性气味的气体。此反应的化学方程式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com