

分析 (1)根据当质子数=核外电子数,为原子,进行分析解答.
(2)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似;据此进行分析解答.
解答 解:(1)原子中,质子数=核外电子数,则12=2+8+x,x=2.
(2)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似;D元素原子的最外层电子数为2,D元素的原子最外层电子数为2,化学性质相似;A原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素,化学性质稳定,故与D元素化学性质不相似.
故答案为:(1)2;(2)D.
点评 本题考查学生对原子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系、元素的化学性质与它的原子的最外层电子数目的关系是解题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+O2↑ | B. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$Hg2+O2↑ | ||
| C. | C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2↑ | D. | 3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
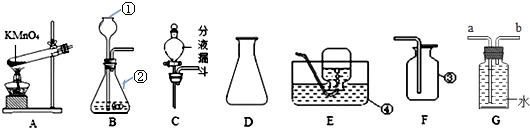
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
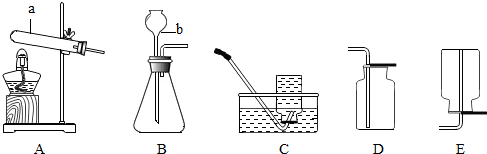
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
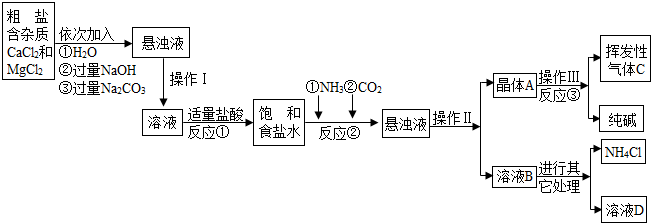
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
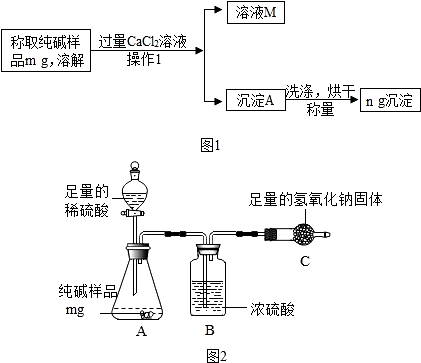
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用过氧化氢溶液和二氧化锰制氧气 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ 分解反应 | |
| B. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| C. | 用铁制容器配波尔多液 Fe+CuSO4═FeSO4+Cu 置换反应 | |
| D. | 用熟石灰制生石灰 CaO+H2O═Ca(OH)2 化合反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com