
【题目】溶液的配制是日常生活和化学实验中的常见操作。硫酸溶液和氨水的密度与其溶质的质量分数对照表如下:(20℃)
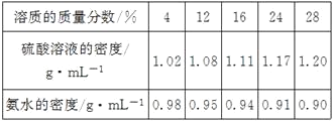
请你仔细分析后回答下列问题:
(1)20 ℃时,随着溶液中溶质的质量分数逐渐增大,氨水的密度逐渐____(填“增大”“减小”或“不变”)。
(2)将100mL溶质的质量分数为16%的硫酸与100mL水混匀后,所得溶液的溶质质量分数____8%(填“>”“<”“=”或“无法判断”)。
科目:初中化学 来源: 题型:
【题目】请根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
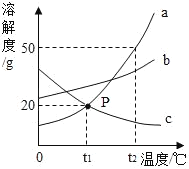
(1)P点的含义是_____。
(2)t2℃时,30g物质a加入到50g水中不断搅拌,得到物质a的_____(填“饱和”或“不饱和”)溶液;此时溶液中溶质的质量分数是_____(精确到0.1%)。
(3)将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数最小的是_____。
(4)物质a中含有少量的物质b,可采取_____的方法提纯a物质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示的实验回答问题:

(1)图甲为酸碱中和反应实验的操作及有关物质质量的变化曲线。则c点时溶液的颜色为_____,b点时溶液中含有的溶质是_____。
(2)图乙为实验室用5%的过氧化氢溶液制取氧气的装置。装置内发生反应的化学方程式为_____,装置中小试管的作用是_____。为配制300g溶质质量分数为5%的过氧化氢溶液需要溶质质量分数为30%的过氧化氢溶液的质量是_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于溶液的说法错误的是( )
A.固体、液体、气体都可以做溶质
B.NH4NO3溶解过程中吸热,溶液温度降低
C.欲使100克KNO3溶液的质量分数由5%变成10%,可向其中加入5克KNO3固体
D.25℃时,将某KNO3溶液蒸发10克水析出a克晶体,再蒸发10克水析出b克晶体,a与b的质量不一定相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】三种固体物质a、b、c的溶解度曲线如图所示,则下列说法不正确的是( )
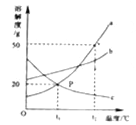
A.t1℃时三种物质的饱和溶液中溶质的质量分数大小为b>a=c
B.a、b、c三种物质的饱和溶液从t2℃降温到t1℃时都有晶体析出
C.t2℃时,将50g a物质加入到100g水中完全溶解形成饱和溶液
D.a中混有少量b时可采取降温结晶的方法提纯得到a
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】医生给病人输液时,常用葡萄糖注射液。如图为葡萄糖注射液的部分标签图,根据图回答下列问题:

(1)每克葡萄糖完全氧化约放出17.2kJ的能量,一瓶这样的葡萄糖注射液可放出_____kJ的能量。
(2)现要配制10kg这种葡萄糖注射液,需用葡萄糖_____kg。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组设计了图的实验,用稀盐酸测定100g被部分氧化的铜样品中铜的含量。请计算:
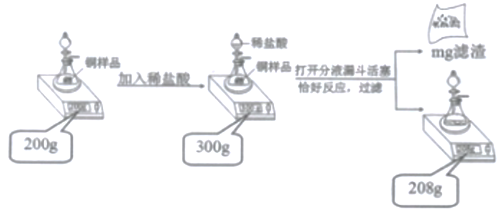
(1)m=________。
(2)所用稀盐酸中溶质的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类宝贵的自然资源。
(1)硬水给生活和生产带来很多麻烦,生活中常用_____的方法降低水的硬度。
(2)氯气可用作自来水的消毒剂,实验室制取氯气的化学方程式为:MnO2+4HCl(浓)![]() X+Cl2↑+2H2O,X的化学式为_____。
X+Cl2↑+2H2O,X的化学式为_____。
(3)在电解水实验中产生氧气和氢气的体积比约为_____。
(4)登山和潜水供氧装置中,过氧化钠(Na2O2)与水反应,生成氢氧化钠和氧气,有关反应的化学方程式为_____
(5)加入适量氯化钡溶液,可以除去盐酸中混有的少量硫酸,有关反应的化学反应方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁钉长期放置在潮湿的环境中会生锈(用Fe2O3表示铁锈)。取5.0g生锈的铁钉放入试管中,用CO还原,充分反应后,称得剩余固体质量为4.4 g。请计算:
(1)生成CO2的质量______;
(2)此铁钉中铁锈的质量分数________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com