
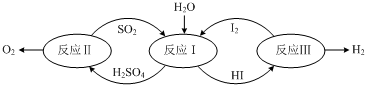
分析 (1)根据反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI进行分析;
(2)根据单质中元素的化合价为零进行分析;根据方程式分析反应的基本类型即可;
(3)根据既是反应物,也是生成物的可以循环使用进行分析;根据质量守恒定律分析解答.
解答 解:(1)由图可知,反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI,化学方程式为:SO2+2H2O+I2=H2SO4+2HI;
(2)反应Ⅲ中,H和I由化合态变为游离态,元素的化合价发生了改变;由图示可知,反应Ⅲ的化学方程式为2HI?H2+I2,发生反应的基本类型为分解反应;
(3)既是反应物,也是生成物的可以循环使用,在整个反应过程中,SO2、H2SO4、I2、HI都在循环使用;根据质量守恒定律可知,制得H2中氢元素最初来源于水;
故答案为:(1)SO2+2H2O+I2═H2SO4+2HI (2)H、I;分解;(3)SO2、I2、H2SO4、HI;H2O.
点评 本题考查化学方程式的书写,元素的化合价等知识,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | ①只能表示氢元素 | |
| B. | ③只能表示铜原子 | |
| C. | ③④⑤能表示物质的化学式 | |
| D. | ②中的“2”表示铁离子带2个单位正电荷 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
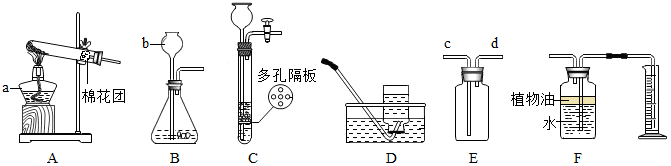 (1)写出下列仪器名称:a酒精灯;b长颈漏斗.
(1)写出下列仪器名称:a酒精灯;b长颈漏斗.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物 质 | 所需时间 | 价 格 |
| 铁屑 | 约13900s | 10.00元/1000g |
| 锌粒 | 约50s | 20.00元/500g |
| 镁片 | 约20s | 10.80元/25g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com