
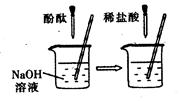
同学们在学习酸和碱的化学性质时,进行了如图所示的实验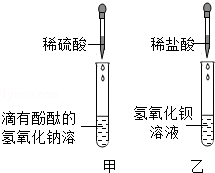
(1)甲实验中能证明两种物质发生反应的明显现象是
(2)实验结束后,同学们将甲、乙两个实验所得的无色废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:硫酸钡、指示剂、水、碱类物质和 (写化学式或名称)
②对碱类物质是什么?同学们有如下猜想
猜想一:只有氢氧化钠
猜想二:只有氢氧化钡
猜想三:是氢氧化钠和氢氧化钡
你认为猜想 是错误的
【实验设计】若要证明剩余的两种猜想,可选用的试剂是
(1)红色溶液变成无色;(2)【交流讨论】①氯化钠或NaCl;②猜想二;【实验设计】硫酸或硫酸钠等可溶性硫酸盐
解析试题分析:(1)酚酞溶液遇碱变红,但是遇到中性和酸性溶液都不变色,硫酸和氢氧化钠反应要生成硫酸钠和水,它们恰好完全反应后的溶液为中性,所以红色要消失;(2)【交流讨论】①甲实验中硫酸和氢氧化钠反应生成硫酸钠和水,而乙实验中盐酸和氢氧化钡反应生成了氯化钡和水,它们混合后,硫酸钠要和氯化钡反应生成硫酸钡沉淀和氯化钠,所以在溶液中还存在着氯化钠;②根据①的解答可以知道,溶液中存在着碱性物质,由于甲实验中氢氧化钠已被完全消耗,如果存在碱性物质,必然是乙实验中过量的氢氧化钡,而氢氧化钡和硫酸钠可以反应生成硫酸钡沉淀和氢氧化钠,所以可以判断在碱性物质一定含有氢氧化钠,至于是不是含有氢氧化钡则应该看硫酸钠的量,也就是说氢氧化钡可能存在也可能不存在,但绝对不能是单纯的氢氧化钡;【实验设计】根据剩余的两种猜想可以知道它们的差别在于是不是含有氢氧化钡,所以只要验证是否含有氢氧化钡即可完成判断,根据氢氧化钡的性质可以用硫酸或硫酸钠等可溶性硫酸盐来进行验证,如果产生了表示沉淀,则证明猜想三正确,如果没有白色沉淀产生,则说明猜想一正确
考点:探究酸碱的主要性质;实验探究物质的组成成分以及含量;酸的化学性质;碱的化学性质


科目:初中化学 来源: 题型:探究题
新课标化学教材九年级上册(2012教育部审定)“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
| Ⅳ分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 | |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
实验是研究物质的性质及其变化规律的重要手段,请根据下述实验内容回答问题。
|

|
|
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
老师请化学兴趣小组的同学帮助他将失去标签的碳酸钠、稀盐酸、氯化钠、氢氧化钠和氯化钙溶液鉴别出来.重新贴好标签.为了区分这五种溶液,将试剂瓶编号为A,B,C,D,E,该小组同学进行了如下探究:
| | 实验步骤 | 实验现象 | 实验结论 |
| 步骤一 | 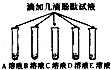 | B,C溶液呈现红色 A,D,E溶液颜色无明显变化 | B,C溶液显 性 |
| 步骤二 | 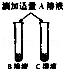 | B,C溶液红色均消失, 且C溶液中产生大量气泡 | 可确定B为 溶液;A与C的反应通常 不用作实验室制取气体的 原因是 |
| 步骤三 | 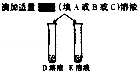 | E中无明显现象, D中的现象为 | 确定E为氯化钠溶液, 则D溶液与所加试剂发生反应的化学方程式为 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样,已知它是无色液体,是初中化学常用的试剂。小强和小华同学很感兴趣,决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 。
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
Ⅱ.Na2CO3和NaHCO3溶液都呈碱性。
Ⅲ.测定室温(20℃)时,四种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中, 滴加氢氧化钙溶液 | | 猜想②正确 相关的化学方程式 |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
以下是某研究小组探究影响反应速率部分因素的相关实验数据.
| 实验序号 | 过氧化氢溶液浓度、% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| 1 | 5 | 1 | 20 | 0.1 | 4 | 16.74 |
| 2 | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| 3 | 30 | 5 | 35 | | 2 | 49.21 |
| 4 | 30 | 5 | 55 | | 2 | 10.76 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题。
Ⅰ.结构:
NaOH含有钠元素,钠在元素周期表中处于第三周期的 (填“开头”、“中间”或“结尾”)。
NaOH属于碱,碱在溶液中都可以电离出相同的离子,该离子是 (填离子符号)。
Ⅱ.制备:
实验室用纯碱制备烧碱的化学反应方程式为 。Ⅲ.性质及变化:
(1)氢氧化钠固体曝露在空气中容易 ,因此它与生石灰一起用作某些气体的干燥剂
(2)如右图所示,NaOH溶液可与稀酸反应的方程式为 。
该反应没有明显的现象,为了说明该反应确实能够发生,下列哪种物质肯定无法帮助你达到目的 。
a.镁条 b.酚酞 c.CuSO4 d.Ba(NO3)2
Ⅳ.保存:
张老师整理药品时,意外发现实验桌上有瓶敞口放置的NaOH固体,他让同学们对这瓶NaOH固体进行探究
【提出猜想】
猜想I:没有变质
猜想Ⅱ:部分变质为Na2CO3,依据是 (用方程式表示);猜想Ⅲ:全部变质
【实验设计、现象和推断】
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
Y型管是实验改进时经常使用的仪器.
(1)用图1所示装置研究可燃物燃烧的条件.已知:白磷的着火点为40℃,红磷的着火点为240℃.
①若在a处放置红磷,在Y型管中可以观察到的现象是 .
②若要研究可燃物燃烧的另一个条件,应在a处加入 .
(2)用图2所示装置可以研究二氧化碳的相关性质.
①在不打开装置的情况下,将Y型管I向右倾斜,使稀硫酸流入碳酸钠中,再恢复至图示装置的角度,即可产生二氧化碳.Y型管II中的现象是 .
②不改换实验仪器,将上述实验进行修改,即可证明二氧化碳的密度大于空气密度.修改方法是 .
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
在学习过程中,可以判断反应发生的方法有多种。
(1)向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com