
【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
[演示实验]将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_____。
[查阅资料] CaC12溶液显中性
[提出问题]实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质的成分是什么?
[猜想与假设]针对疑问,甲组同学猜想如下:
猜想I:只有CaC12
猜想II:有_____
猜想III:有CaC12和Ca (OH)2
猜想IV:有CaCl2、HC1 和Ca (OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是_____。
[实验探究]为了验证其余猜想,各小组进行了下列三个方案的探究。
实验方案 | 滴加紫色石蕊溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | _____ | _____ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca (OH)2 | 溶液中含有Ca (OH)2 | 溶液中含有Ca (OH)2 |
[得出结论]通过探究,全班同学一致确定猜想III是正确的。
[评价反思]
(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca (OH)2,请你帮助他们说明原因_____。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑_____。
【答案】![]() CaCl2和HC1 HC1和Ca(OH)2不能共存 石蕊溶液变蓝 溶液变浑浊 因为碳酸钠与氯化钙也能产生碳酸钙白色沉淀 反应物是否有剩余
CaCl2和HC1 HC1和Ca(OH)2不能共存 石蕊溶液变蓝 溶液变浑浊 因为碳酸钠与氯化钙也能产生碳酸钙白色沉淀 反应物是否有剩余
【解析】
[演示实验]
稀盐酸和氢氧化钙反应生成氯化钙和水,化学方程式为:![]() ,故填:
,故填:![]() ;
;
[猜想与假设]
盐酸和氢氧化钙反应存在三种情况;
稀盐酸和氢氧化钙溶液恰好完全反应溶质为CaCl2
稀盐酸和氢氧化钙溶液反应盐酸过量溶质为CaCl2和HC1
稀盐酸和氢氧化钙溶液反应氢氧化钙过量溶质为CaC12和Ca (OH)2
故填:CaCl2和HC1;
乙组同学对以上猜想提出质疑,认为猜想IV不合理因为HC1 和Ca (OH)2会反应不共存,故填:HC1 和Ca (OH)2不共存;
[实验探究]
(1)溶液中含有Ca (OH)2滴加紫色石蕊会变蓝,故填;石蕊溶液变蓝;
(2)二氧化碳和氢氧化钙反应生成碳酸钙和水,溶液中含有Ca (OH)2通入二氧化碳,澄清石灰水会变浑浊,故填:溶液变浑浊;
[评价反思]
(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca (OH)2,因为CaCl2也可以和Na2CO3溶液产生白色沉淀,故填:因为碳酸钠与氯化钙也能产生碳酸钙白色沉淀;
(2)综上所述以后再分析反应后所得溶液中溶质的成分时,除了考虑生成物外.还需要考虑反应物是否有剩余,故填:反应物是否有剩余。


科目:初中化学 来源: 题型:
【题目】每年的 CES(国际消费类电子产品展览会)都会有一大波“黑科技”产品发布, 而这些产品大多是由金属材料制成,铜是其中重要的金属材料。
I.自然界中的铜主要以化合物形式存在于铜矿石中,从“绿色化学”的理念分析,以下铜矿最适宜炼铜的是_____(填序号)
A 黄铜矿(CuFeS2) B 辉铜矿(Cu2S)
C 蓝铜矿 [Cu(OH)2(CO3)2 ] D 斑铜矿(Cu5FeS4)
II.某化学兴趣小组用如下实验装置制取一氧化碳,再用一氧化碳还原氧化铜模拟炼铜。
(查阅资料)
(1)实验室常用甲酸(H2CO2)和浓硫酸混合加热制备 CO,同时生成 H2O。
(2)浓硫酸具有吸水性。
(进行实验)小组同学组装好下图装置并检查装置气密性之后开始实验,先让 A 装置反应一会儿,然后熄灭 A 中的酒精灯,再点燃 C 装置中的酒精灯。
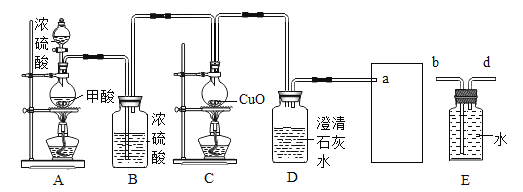
(1)装置 B 的作用是_____;装置 C 中发生反应的化学方程式是_____。
(2)装置 D 的作用是_____;该装置的组装存在的错误是_____; 改正之后,该装置中发生反应的化学方程式是_____。
(3)为避免一氧化碳污染空气,回收利用一氧化碳,方框中应连接装置 E,与 a 导管接口相接的是_____(填“b”或“d”)。
(4)实验结束之后,得到带有金属光泽的砖红色粉末,小组决定对该固体的成分进行探究。
(提出问题)红色的固体是什么?
(查阅资料)氧化亚铜(Cu2O)是红色粉末状固体;
会与稀硫酸反应:Cu2O + H2SO4 == CuSO4 + Cu + H2O。
(提出猜想)猜想一:该固体全部为 Cu;
猜想二:该固体全部为 Cu2O;
猜想三:该固体为 Cu2O 和 Cu 的混合物。
(实验方案)
实验步骤 | 实验现象及实验结论 |
取少量固体粉末于试管中, 加入过量_____溶液。 | 若无明显变化,则猜想一成立; 若溶液变为_____色,则猜想二或猜想三成立。 |
为了进一步确定混合物的组成,另取 m g 固体,重复上述实验,然后将反应后的物质过滤、洗涤、干燥,再次称量得到 n g 固体,若 m 和 n 满足_____的量的关系,则 猜想三成立。
(得出结论)该固体为 Cu2O 和 Cu 的混合物。
(交流讨论)
(1)从实验安全的角度考虑,本实验存在的危险是_____,改进的方法是_____;
(2)从物质的转化程度考虑,小组同学针对如何将氧化铜全部转化为铜单质展开讨论, 查阅了大量资料之后知道,反应条件是影响生成物的重要因素,因此一致认为在下次实验中需要适当加大 CO 的通入量或者_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表列出了硝酸钾在不同温度时的溶解度.
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
某兴趣小组做了以下实验:

(1)上述溶液中的溶剂是________,上述实验过程中得到的溶液一定属于不饱和溶液的是________(填数字序号),⑤所对应的实验现象是________.
(2)实验过程中,溶质的质量分数一定相等的是________(填数字序号).
(3)为了防止水体污染,小组同学提出了如下方案处理实验后的废液: 步骤I:将⑤继续冷却至0℃,过滤,共可回收得到KNO3固体________g.
步骤II:向滤液中加入________g水稀释,得到溶质的质量分数为1%的KNO3稀溶液,将此溶液做为化肥使用.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种环保型杀菌消毒剂。在生活中主要用于饮用水的消毒和食品保鲜。用二氧化氯消毒后的水可以直接饮用。
二氧化氯是一种黄绿色、有刺激性气味的有毒气体,密度比空气大,其熔点为-59℃,沸点为11.0℃,易溶于水,且与水反应得到酸性溶液。该气体具有强烈的腐蚀性,吸入高浓度二氧化氯气体会引起咳嗽和呼吸道粘膜的损伤。
二氧化氯极其不稳定,受热或见光易发生爆炸性分解,直接造成氯气泄漏而污染环境,所以只有依靠现场制备。工业上用稍潮湿的氯酸钾(KClO3)和草酸(H2C2O4)在60℃时反应制得。由于制取二氧化氯需要使用的氯酸钾是易爆危险品,所以制备和运输成本很高,因此我国目前还未广泛用其消毒自来水。
请依据文章回答下列问题:
(1)本文介绍了二氧化氯的性质、制法和____________等方面内容。
(2)二氧化氯的化学性质有①_______________________;②_________________________。
(3)请将制备二氧化氯反应的化学方程式填写完全:
2KClO3 + 2H2C2O4![]() 2ClO2↑+ 2CO2↑ + K2C2O4 + __________
2ClO2↑+ 2CO2↑ + K2C2O4 + __________
(4)发生二氧化氯泄漏时,紧急处理方法是__________________________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】选择下列部分实验操作可完成两个实验,甲实验为除去粗盐中难溶性的杂质,乙实验为配制溶质质量分数为10%的氯化钠溶液。下列说法正确的是( )
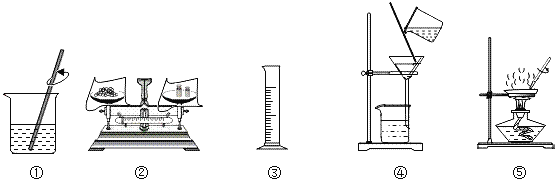
A. 操作①和⑤中玻璃棒的作用是相同的
B. 甲实验和乙实验都要用到的实验操作①
C. 甲实验在操作⑤时,将水全部蒸发后停止加热
D. 乙实验在操作③时,若俯视读数,会使所配制溶液的溶质质量分数偏小
查看答案和解析>>
科目:初中化学 来源: 题型:
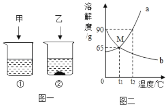
【题目】t2℃时,将甲、乙各80g分别放在盛有100g水的两个烧杯中,充分溶解后,恢复到t2℃,现象如图一,甲和乙的溶解度曲线如图二。请结合图示回答下列问题:
(1)固体甲对应的溶解度曲线是_____(填“a”或“b”)。
(2)M点的含义_____。
(3)向烧杯①的溶液中继续加入15g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分甲析出,你认为“全部溶解”的原因是_____。
(4)将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,所得溶液的有关说法正确的是_____(填字母)。
a.甲溶液仍为饱和溶液 b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙 d.两溶液溶质质量分数甲>乙。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文:
尿素,是一种白色晶体,化学式为CO(NH2)2,它是目前使用量最大的一种化学肥料。尿素是蛋白质在体内代谢的产物。早在1737—1785年,德国医生博哈夫和法国实验员鲁埃分别通过蒸发尿液获得了尿素。尿素在土壤中酶的作用下,转化为碳酸铵或碳酸氢铵,才能被作物吸收利用,在土壤中不残留任何有害物质,长期施用没有不良影响,而具有相同服效的硫酸铵化肥,如果长期施用,就会使土壤酸化、板结。
依据以上信息,回答下列问题:
(1)按照化肥的分类,尿素属于__________(填“氮”“磷”“钾”或“复合”)肥。
(2)中氮元素的质量分数 _______________________________(列计算式即可)。
(3)蒸发尿液可获取尿素,由此可以推断尿素的化学性质是______________________(写一条)。
(4)尿素转化为碳酸氢铵,该转化属于_____________(填“物理变化”或“化学变化”)。
(5)下列说法正确的是______(填序号)。
a 蛋白质在体内代谢产物之一为尿素
b 尿素施用在土壤中,能够被作物直接吸收
c 尿素、碳酸氯铵、碳酸铵都属于有机化合物
d 硫酸铵和熟石灰混合施用,可提高肥效
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如表是国家对“饮酒驾车”和“醉酒驾车”的界定标准。
饮酒驾车 | 20mg/100mL≤血液中的酒精含量<80mg/100mL |
醉酒驾车 | 血液中的酒精合量≥80mg/100mL |
白酒、酒精和啤酒中均含有乙醇(俗称酒精,化学式为C2H5OH),饮酒后酒精可进入人体血液中。回答下列问题:
(1)乙醇分子中碳、氢、氧各原子个数比为_______,其中碳、氢元素的质量比是_______;
(2)乙醇中碳元素的质量分数为_______。(结果精确到0.1%)。
(3)饮酒会使人的神经系统过度兴奋或麻痹抑制,容易引发交通事故。某人饮酒后驾 车,被交警发现,经测定其每10mL血液中酒精含量为9.3mg,属于_______驾车。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com