
【题目】奶油的主要成分为脂肪和蛋白质,还富含维生素A(C20H30O),呈弱酸性。
(1)奶油是一种高热量食品,原因是成分中富含_______________和蛋白质。
(2)蛋白质中一定含有氢、氧、________和____________元素。
(3)维生素A中碳元素:氢元素质量比________。
(4)奶油的pH约为_________(填序号)
a 0.2 b 6.6 c 7.3 d 14.0
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:
【题目】今年“五·一”假期,小丽随爸爸到乡下省亲,期间看到许多漂亮的大理石。于是她带了一些回来,想去学校实验室测定这些大理石中碳酸钙的含量。她称取了20克大理石样品置于烧杯中,然后将250g稀盐酸分成五等份,依次加入烧杯充分反应,记录有关实验数据如下表所示(大理石中其他成分均不溶于水,也不参与化学反应)。
加入次数 | 一 | 二 | 三 | 四 | 五 |
加入稀盐酸的质量/g | 50 | 50 | 50 | 50 | 50 |
烧杯中剩余固体的质量/g | 15 | 10 | 5 | 5 | m |
试求:(1)m的值应为_____;
(2)实验中大理石样品所含碳酸钙的质量分数?
(3)实验中所用稀盐酸的溶质质量分数?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E分别是锌、硫酸、氢氧化钡、硫酸铜和碳酸钠五种物质中的一种,如图所示:

“﹣”表示相连的两种物质能够发生反应,其中D的溶液呈蓝色,A与B反应生成的气体是光合作用的原料之一。
(1)D的化学式是 。
(2)A与B反应的化学方程式 。
(3)C与D反应的化学方程式 ,属于基本反应类型中的 。
(4)下列可以替代E的是 (填序号)。
①氯化铜 ②氢氧化钾 ③银
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产二水合氯化钙(CaCl2·2H2O)流程如下。原料石灰石中含有的杂质主要是MgCO3、SiO2和Fe2O3。

(1)第①步酸洗所用的酸是____________(填编号)。
A 稀盐酸 B 稀硫酸 C 浓硫酸 D 稀硝酸
(2)酸洗时酸与Fe2O3反应的化学方程式是______________。
(3)固体1的名称是__________。
(4)实验室中操作Ⅰ所用到的玻璃仪器有:玻璃棒、烧杯、__________。
(5)操作Ⅱ的名称是:蒸发浓缩、__________、__________。
(6)该流程中可循环利用的物质是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1是a、b、c三种物质的溶解度曲线,据图回答下列问题:
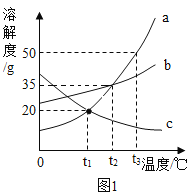
①三种物质的溶解度随着温度升高而减小的物质是_____。
②t3℃时,a物质的溶解度为_____。
③t1℃时,把50g物质a加入到200g水中充分搅拌、静置,所得溶液的质量为_____g。
④c的不饱和溶液变成饱和溶液的方法是_____(写一种)。
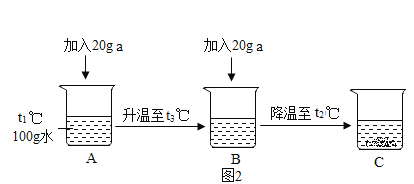
⑤取固体a进行如图2实验,一定属于饱和溶液的是_____,溶质质量分数最大的是_____,烧杯C中溶质的质量分数为_____(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CaCO3在生产生活中有广泛的用途。
(1)烧石灰石可制得活性CaO,反应的化学方程式为_________________________。为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等份,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图所示。由此可知:CaO与水反应会__________热量(填“放出”或“吸收”),上述温度中,_________℃煅烧所得CaO活性最高。

(2)以电石渣[主要成分为Ca(OH)2还含有少量MgO等杂质]为原料制备高纯CaCO3的流程如下:
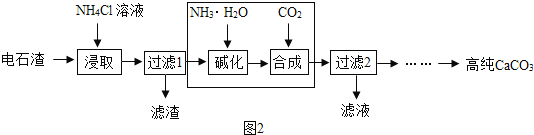

①上图为NH4Cl浓度对钙、镁浸出率的影响(![]() ),为进一步提升CaCO3的产量和纯度,据图分析,较适宜的NH4Cl溶液的质量分数为_______,浸取时主要反应的化学方程式为______________________________。
),为进一步提升CaCO3的产量和纯度,据图分析,较适宜的NH4Cl溶液的质量分数为_______,浸取时主要反应的化学方程式为______________________________。
②流程中框线内若改用溶液_________________(填化学式),可一步得到与原流程完全相同的生成物。
③流程中框线内若改用Na2CO3溶液,也能得到高纯CaCO3。试从生成物的角度分析原流程的优点:a.NH3可循环利用;b._______;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国是海洋大国,浩瀚的海洋为我们提供了丰富的资源,为了保卫我们神圣的海权,近年来我国对南海部分岛礁进行了吹填扩建,为海洋资源的开发利用提供了便利条件。
(1)我们的食用盐大部分来自于海水,从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,可以将粗盐溶于水,然后进行如下操作:
①加过量的Ba(OH)2溶液;②加适量的盐酸;③加过量的Na2CO3溶液;④过滤;⑤蒸发。正确的操作顺序是_______(填字母)。
(2)如图是氯化钠、氢氧化钠两种固体物质的溶解度曲线。
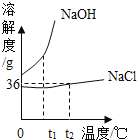
①t1℃时,NaCl饱和溶液中溶质质量分数________NaOH饱和溶液中溶质质量分数(填“大于”、“小于”、“等于”之一)
②t2℃时,将 20gNaCl固体投入 50g水中,充分溶解后可得到NaCl的_____(填“不饱和溶液”或“饱和溶液”,此时所得溶液的质量是________g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】青一和立信两校化学兴趣小组同学联合举行了“众携手、共探究”的活动。他们设计了如图所示的实验装置(装置气密性良好),进行了以下实验。作为其中一员的你,请根据所学知识回答下列问题:
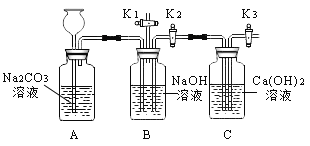
(1)先关闭活塞 K2 和K3,打开活塞 K1。通过长颈漏斗向 A 装置内加入足量的稀盐酸。你认为打开活塞 K1的目的是_____。
(2)然后打开 K2 和 K3,关闭 K1。你可以观察到装置 C 中的实验现象为_____。
(3)一段时间后,将装置 A、B、C 中的所有物质倒入一洁净的废液缸中,充分反应,过滤,得到白色沉淀甲和无色滤液乙。
①白色沉淀甲是_____(填化学式)。
②无色滤液乙中一定不存在的溶质是_____(填化学式)。
③无色滤液乙中的溶质成分可能有很多种组成情况:其中所含溶质种类最少时,请写出所有溶质的化学式_____;其中所含溶质种类最多时,请写出所有溶质的化学式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硝酸钾在不同温度下的溶解度数据如下表所示:
温度/℃ | 0 | 20 | 40 | 60 | 80 |
溶解度(g/100g水) | 13.3 | 31.6 | 63.9 | 110 | 169 |
回答下列问题:
①硝酸钾的溶解度随温度升高而___(填“增大”或“减小”)。
②20℃时,将15克硝酸钾加入40克水中,充分搅拌,所得溶液为____(填“饱和”或“不饱和”)溶液;此时溶液的溶质质量分数为______(列出计算式)。
③某硝酸钾固体中混有少量氯化钠,分离提纯硝酸钾的操作是配成高温下的硝酸钾饱和溶液、_______、过滤、洗涤、干燥。
④甲是60℃的硝酸钾溶液,按下图所示进行操作。分析正确的是____(填序号)。
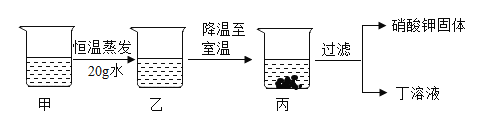
A 乙一定是不饱和溶液
B 丙和丁一定是饱和溶液
C 乙的溶质质量分数不一定比甲大
D 甲和丙的溶质质量分数有可能相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com