
硫铁矿[主要成分是二硫化亚铁(FeS2)],其他成分不含铁,硫元素是一种重要的化工原料,常用来制备硫酸和氯化铁,工业生产流程如图所示。
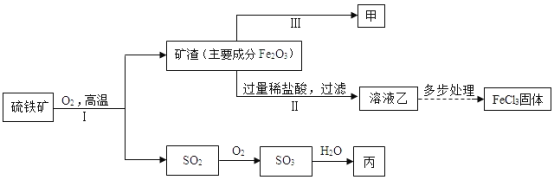
(1)过滤中玻璃棒的作用 _____。
(2)步骤二中主要反应的化学方程式为 _____。
(3)溶液乙中一定有的阳离子_____。
(4)上述流程中所涉及的含硫的物质中,硫元素的化合价共有_____种。
科目:初中化学 来源:2019江西省中考信息模拟化学试卷 题型:科学探究题
化学兴趣小组探究金属与酸反应时,小珍同学将浓硫酸与铜片混合物溶液加热,一段时间后,观察到溶液变蓝色,同时闻到刺激性气味。
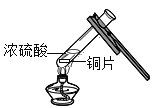
[提出问题]铜能与浓硫酸反应,反应生成的刺激性气味的气体是什么?
[猜想与假设]
猜想1:可能是二氧化硫。
猜想2:可能是__________。
猜想3:可能是二氧化硫与三氧化硫。
猜想4:可能是氯化氢气体。
大家讨论后认为猜想4不合理,依据是__________。
[查阅资料]SO2和SO3都能与氢氧化钡反应生成白色沉淀浑浊。硫酸钡不溶于酸,亚硫酸钡沉淀溶于稀盐酸或稀硝酸反应生成有刺激性气味的气体。
[实验探究]如图所示,小珍将浓硫酸与铜片混合物加热,将产生的气体通入足量的氢氧化钡溶液中,观察到的现象是_______,停止加热,用注射器向装置B中注入足量的稀盐酸,观察到的现象是____________。
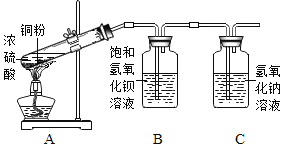
[实验结论]猜想1正确。
[反思拓展]①铜与浓硫酸加热反应生成一种硫酸盐和两种氧化物,写出铜与浓硫酸反应化学方程式:_____。
②C装置的作用是_________。
③铜与稀硫酸加热不发生反应,铜与浓硫酸加热能反应,由此得出的结论是_____(填序号)。
A 浓硫酸与稀硫酸的化学性质不同
B 铜能与稀盐酸反应
C 浓硫酸与铜反应体现了浓硫酸酸性
D 铜与浓硫酸反应证明铜活动性在氢前面
查看答案和解析>>
科目:初中化学 来源:2020年5月湖北省黄石市中考模拟化学试卷 题型:单选题
空气是我们每天都呼吸的“生命气体”。下列说法错误的是( )
A. 空气中氮气的质量分数为 78%
B. 空气中氧气能供给呼吸和支持燃烧
C. 空气中二氧化碳是造成温室效应的气体之一
D. 空气中的稀有气体所占比例虽小,但用途广泛
查看答案和解析>>
科目:初中化学 来源:2020年江苏省扬州市(扬州教育学院附属中学)中考一模化学试卷 题型:单选题
人体内的一些液体正常pH范围如下,其中呈酸性的是
A. 血浆7.35-7.45 B. 胆汁7.1-7.3
C. 胃液0.9-1.5 D. 胰液7.5-8.0
查看答案和解析>>
科目:初中化学 来源:2020年重庆市中考二模化学试卷 题型:单选题
下列所示的四个图象能正确反映对应变化关系的是( )
A.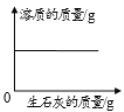 向一定量的饱和石灰水中不断加入生石灰
向一定量的饱和石灰水中不断加入生石灰
B.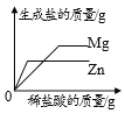 向等质量的镁和锌中加入稀盐酸至过量
向等质量的镁和锌中加入稀盐酸至过量
C.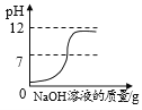 向pH=2的稀盐酸中加入pH=12的氢氧化钠溶液
向pH=2的稀盐酸中加入pH=12的氢氧化钠溶液
D.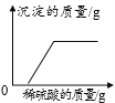 向一定量的氢氧化钾和氯化钡的混合溶液中滴加稀硫酸
向一定量的氢氧化钾和氯化钡的混合溶液中滴加稀硫酸
查看答案和解析>>
科目:初中化学 来源:2020年重庆市中考二模化学试卷 题型:单选题
我国的北斗导航卫星系统采用铷原子钟,提供精确时间。如图是铷元素在元素周期表中的相关信息,下列说法错误的是( )
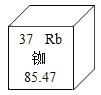
A.铷元素属于金属元素
B.铷元素的相对原子质量约为质子数和中子数之和
C.铷原子的质子数等于中子
D.铷元素的原子序数为37
查看答案和解析>>
科目:初中化学 来源:四川省成都市2019-2020学年九年级上学期12月月考化学试卷 题型:填空题
选择氧气、氢气、二氧化碳、一氧化碳的化学式填空:
(1)有毒的气体是_________;
(2)能用于灭火的气体是________;
(3)对环境保护最理想的燃料是________;
(4)不能燃烧,但能支持燃烧的气体是_______;
(5)同时具有可燃性和还原的的气体是________。
查看答案和解析>>
科目:初中化学 来源:2020年山东省潍坊市诸城市中考一模化学试卷 题型:科学探究题
某化学兴趣小组的同学,通过咨询老师准备用亚硫酸钠溶液与浓硫酸反应来制备一定量的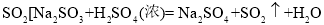 ]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
]。老师给他们提供了一瓶亚硫酸钠溶液并告知该瓶溶液放置时间可能较长,不知是否变质。兴趣小组的同学分成甲、乙两小组对该瓶亚硫酸钠溶液成分进行实验探究。
[提出问题]该瓶溶液中溶质的成分是什么?该瓶溶液中亚硫酸钠的质量分数是多少?
[查阅资料]
a、Na2SO3有较强还原性,在空气中易被氧气氧化: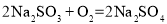 ;
;
b、Na2SO3能与酸反应产生SO2气体;
c、SO32-、SO42-均能与Ba2+反应产生白色沉淀,BaSO3可溶于稀盐酸。
[作出猜想]
猜想1:没有变质,成分是Na2SO3;
猜想2:完全变质,成分是Na2SO4;
猜想3:部分变质,成分是Na2SO3和Na2SO4。
[实验探究I]甲组设计实验探究溶液是否变质:
甲组 | 实验操作 | 现象 | 结论 |
步骤1 | 取少量样品于试管中加入过量稀盐酸。 | 产生气泡 | 溶液中含有_____ |
步骤2 | _____ | _____ | 溶液中含有Na2SO4 |
实验结论是_____。
[实验探究Ⅱ]乙组设计如下实验测定Na2SO3溶液的溶质质量分数。
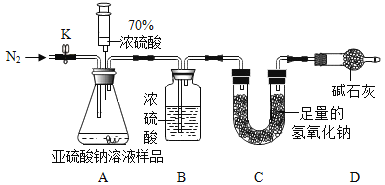
(1)连好装置并检查装置气密性,在锥形瓶中放人126g该样品,通入N2的目的是_____。
(2)实验前称量C装置的质量为128.8g。
(3)关闭活塞K,用注射器推入浓硫酸至不再产生气泡,注射器可以换为_____,也能控制液体试剂的滴加速率。
(4)打开活塞K,缓缓鼓入一定量的N2,继续通入N2的作用是_____。
(5)再次称量C装置的质量为135.2g。
(6)计算出该溶液中Na2SO3的质量分数为10%,若没有D装置,实验结果将_____(填“偏大”“不变”或“偏小”)。
[反思]由此可得出,保存亚硫酸钠时应_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com