
【题目】进行如下实验,研究物质的性质。

(1)A中有气泡产生,证明黄铜为_______合金(填序号)。
a 铜锌 b 铜银 c 铜碳
(2)B中反应的化学方程式为_______。
(3)验证鸡蛋壳中含有碳酸盐,应补充的操作及观察到现象是________。
【答案】a Ca(OH)2+2HCl=CaCl2+2H2O 将产生的气体通入澄清的石灰水中,石灰水变浑浊
【解析】
(1)A中有气泡产生说明黄铜片能和稀盐酸发生反应,即黄铜片里面需要有氢前金属,在a中锌是氢前金属可与稀盐酸酸反应生成氢气,能满足实验现象;b中都是氢后金属,都不与稀盐酸反应,不满足实验现象;d中铜是氢后金属,碳不与稀盐酸反应,不满足实验现象。故填a。
(2)氢氧化钙的俗称是熟石灰,氢氧化钙和稀盐酸反应生成氯化钙和水,反应的化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;故填:Ca(OH)2+2HCl=CaCl2+2H2O。
(3)碳酸盐能与酸反应生成能使澄清石灰水变浑浊的二氧化碳气体,检验碳酸盐最简单的方法是滴加盐酸,观察是否有能使澄清石灰水变浑浊的气体产生,所以应补充的操作是将产生的气体通入澄清的石灰水中,石灰水变浑浊;故填:将产生的气体通入澄清的石灰水中,石灰水变浑浊。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是( )

A. t1℃时,a、c两种物质饱和溶液的溶质质量分数为20%
B. 将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法
C. 将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c
D. 将150g a物质的饱和溶液从t3℃降温至t1℃,可析出30g a物质
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学为探究碱的性质,对氢氧化钙进行如下实验。
(1)将石蕊试液滴入澄清石灰水中,振荡,溶液呈____色。
(2)将稀盐酸逐滴加入含有酚酞试液的石灰水中,振荡,可观察到什么现象?____
(3)将CO2气体通入澄清石灰水中,澄清石灰水变浑浊,说明氢氧化钙能与某些___(填物质类别)反应,氢氧化钙与氢氧化钠的化学性质相似,试写出三氧化硫与氢氧化钠反应的化学方程式___。
(4)向氢氧化钙和稀盐酸反应后的溶液中逐滴滴加Na2CO3溶液,溶液pH的变化如图所示,e点溶液中溶质的化学式是___,滴入Na2CO3溶液的过程中d~m段观察到的现象是____,m~n段观察到的现象是___。

(5)称取5g含有氯化钠杂质的氢氧化钠样品,加入25g水后充分溶解,缓慢加入10%的稀盐酸,当溶液的pH=7时,刚好用去稀盐酸的量为36.5g。计算样品中氢氧化钠的质量分数____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
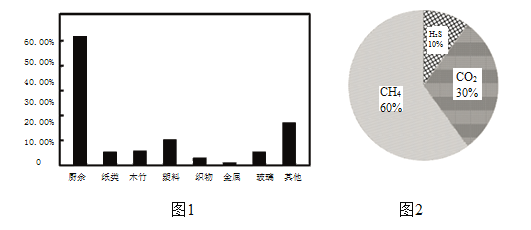
随着生活水平的提高,生活垃圾也变得越来越多。2018年北京市生活垃圾各组分所占比例如图所示。
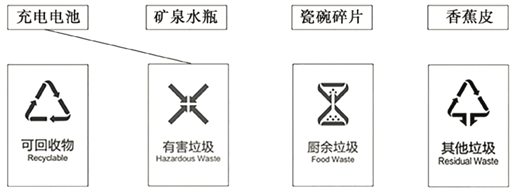
《北京市生活垃圾管理条例》将生活垃圾分为四类,并采用不同颜色的垃圾桶进行区分:厨余垃圾(绿色)、可回收物(蓝色)、有害垃圾(红色)和其他垃圾(灰色)。
类别 | 主要包括 |
厨余垃圾 | 菜帮菜叶、瓜果皮壳、鱼骨鱼刺、剩菜剩饭、茶叶渣等 |
可回收物 | 废玻璃、废金属、废塑料、废旧织物、废纸张、废书籍等 |
有害垃圾 | 充电电池、温度计、消毒液、含汞荧光灯管、过期药品、杀虫剂等 |
其他垃圾 | 卫生纸、塑料袋、纸尿裤、餐盒、大棒骨、陶瓷碎片等 |
垃圾分类不仅有助于降低垃圾混合处理所带来的污染问题,还能提高垃圾处理的针对性。如厨余垃圾通过厌氧发酵法转化为沼气,主要成分如图所示,经过提纯处理后,可制成CNG压缩天然气,CNG中CH4含量≥97%。
垃圾分类需要每一个人的支持与参与。
依据文章内容,回答下列问题:
将下列物质与应投入的垃圾桶连线_______。
(2)沼气的主要成分为甲烷(CH4),甲烷完全燃烧的产物是_______。
(3)垃圾分类的意义有_______(写出一条)。
(4)厨余垃圾转化为沼气的方法是_______。
(5)下列说法正确的是_______。
A 2018年北京市生活垃圾中厨余垃圾所占比例最高
B 北京生活垃圾分为四类,用不同颜色的垃圾桶区分
C 沼气制成CNG压缩天然气,主要去除了H2S、CO2
D “光盘行动”有助于减少厨余垃圾
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某炼锌厂利用含ZnO的烟尘处理硫酸厂烟气中的SO2。

(1)下列物质中属于氧化物的是_______(填字母序号)。
A ZnO
B SO2
C ZnSO3
D ZnSO4
(2)ZnSO3 与废酸中的H2SO4反应的化学方程式为_______。
(3)过程II产生的SO2可用于制备硫酸,化学方程式可表示为:![]() 64g SO2完全反应理论上可制得H2SO4的质量为_______g。
64g SO2完全反应理论上可制得H2SO4的质量为_______g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】上右图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )

A. t2℃时,甲、乙两种物质的溶解度相等
B. 甲的溶解度随温度的升高而增大
C. 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙
D. t1℃时,丙的饱和溶液中溶质的质量分数为40%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)小明要用100g质量分数为10%的氢氧化钠溶液来制作“叶脉书签”,如图是他配制氢氧化钠溶液的实验操作示意图.
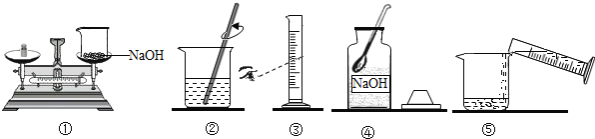
①量取所需要的水应选择_______(选填“10mL”、“50mL”或“100mL”)量筒.
②指出图中的2处操作错误,请写出其中的一处错误:________.
③用上述图示的序号表示配制溶液的操作顺序:_________.
④配置100g质量分数为10%的氢氧化钠溶液,需要氢氧化钠_______g.如果按图中③量取水的质量______(填“偏小”或“偏大”或“不变”)
(2)现用质量分数为12%的氢氧化钠溶液(密度约为1.09g/cm3)配置20g质量分数为6%的氢氧化钠溶液,需要质量分数为12%的氢氧化钠溶液________mL(计算结果精确到0.1),需要水_______mL(水的密度为1g/cm3)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成。用它制备氢氧化镁的流程示意图如下:

部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
(1)熟石灰主要成分的化学式是____________。
(2)溶液A中的阳离子是___________________(填离子符号)。
(3)沉淀C的成分是_____________________。
(4)溶液B与熟石灰反应的化学方程式是____________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铁矿的主要成分是二硫化亚铁(FeS2),其中硫元素的化合价为-1.由黄铁矿为原料生产硫酸的工业流程如下图所示。

(1)生产的第一步将黄铁矿粉碎的目的是_____;
(2)生产的第二步是在接触室内将SO2转化成SO3,反应的化学方程式为_____;
(3)在生产过程中,化合价发生改变的元素有_____种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com