
| 食物 | 葡萄 | 牛奶 | 苹果 | 豆制品 |
| pH | 3.5一4.5 | 6.3-6.6 | 2.9-3.3 | 7.4一7.9 |
| A. | 豆制品 | B. | 苹果 | C. | 牛奶 | D. | 葡萄 |
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂质的试剂和方法 | |
| A | NaOH | Na2CO3 | 加入适量的稀盐酸,蒸发 |
| B | CaO | CaCO3 | 高温煅烧后冷却 |
| C | FeCl2 | CuCl2 | 溶解,过滤,蒸发 |
| D | Zn | Cu | 加入足量稀盐酸后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③⑤ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
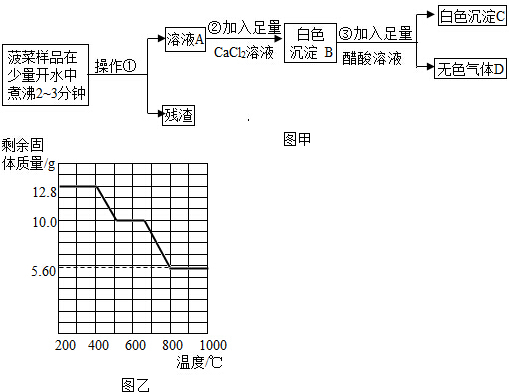
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
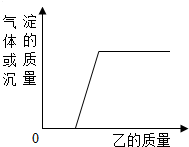 向下表中的甲物质中逐滴加入相应的乙溶液至过量.反应过程中产生的气体或沉淀的质量与加入乙的质量关系,不符合如图曲线描述的是( )
向下表中的甲物质中逐滴加入相应的乙溶液至过量.反应过程中产生的气体或沉淀的质量与加入乙的质量关系,不符合如图曲线描述的是( )| 序号 | 甲 | 乙 |
| 1 | 硝酸和硝酸镁的混合溶液 | 氢氧化钾溶液 |
| 2 | 铜和锌的合金 | 稀硫酸 |
| 3 | 久置空气中的铝片 | 稀盐酸 |
| 4 | 含有碳酸钠的氢氧化钠溶液 | 稀硝酸 |
| 5 | 盐酸和硫酸的混合溶液 | 硝酸钡溶液 |
| A. | 2、5 | B. | 1、3、4 | C. | 1、2、4 | D. | 1、3、5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 莽草酸中氢元素的质量分数最大 | B. | 莽草酸由碳、氢、氧三种元素组成 | ||
| C. | 莽草酸中各元素的质量比为7:10:5 | D. | 每个莽草酸分子里含有5个氢分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
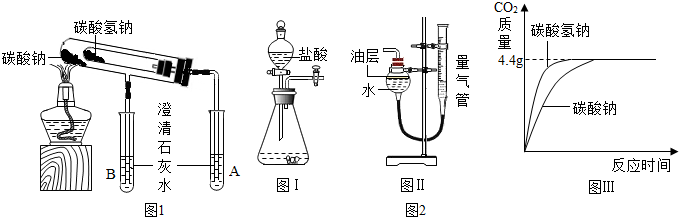
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
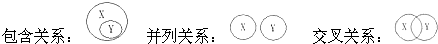
| A. | 纯净物与混合物属于包含关系 | B. | 分解反应与置换反应属于交叉关系 | ||
| C. | 化合物与氧化物属于包含关系 | D. | 氧化反应与化合反应属于并列关系 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com